一般にソーダ灰として知られる炭酸ナトリウムは、無機化合物です。炭酸水素ナトリウムと炭酸ナトリウムを含む複塩であるトロナから抽出されます。塩水が湖のほとりで蒸発する一連のプロセスを経て作られます。
それはしばしば洗濯ソーダと呼ばれ、すべての基本的な重化学物質の中で最も重要です. 炭酸ナトリウムは水に溶けます。 水酸化ナトリウムに対する炭酸ナトリウムの大きな利点は、炭酸ナトリウムが非腐食性であることです。したがって、より安全に処理できます。
炭酸ナトリウムの用途は何ですか?
炭酸ナトリウムにはさまざまな用途があります。それらのいくつかは次のとおりです:
<オール>炭酸ナトリウムの形成
炭酸ナトリウムの形成にはいくつかのステップがあります。それらは次のとおりです:
<オール>NaCl+H2O+CO2+NH3→NH4Cl+NaHCO3
- 次のステップで、重炭酸ナトリウムは炭酸ナトリウムに分解されます
2 NaHCO3 → Na2CO3 + H2O + CO2
注: [Na+] x [HCO3] のイオン積> NaHCO3 の ksp
しかし、炭酸ナトリウムは水に溶けるので、KHCO3 は Solvay プロセスでは調製できません。
必須化合物の特性 – 炭酸ナトリウム
重要な化合物である炭酸ナトリウムには、いくつかの物理的および化学的特性があります。それらは以下にリストされています:
炭酸ナトリウムの物性は以下の通りです。
- 炭酸ナトリウムの式は Na2CO3 です
- 炭酸ナトリウムの分子量は 105.9888g/mol、炭酸ナトリウムの密度は 2.54g/cm3
- 炭酸ナトリウムの沸点は160℃、融点は851℃
- 炭酸ナトリウムは無臭です
- 炭酸ナトリウムは白色の結晶性固体です
- 炭酸ナトリウムは水に溶けます。
炭酸ナトリウムの化学的性質は次のとおりです。
- 希塩酸との反応 –
Na2CO3 + 2HCl 希釈 → 2NaCl + CO2+ H2O
- 水と二酸化炭素 (炭酸水素ナトリウムの調製用)–
Na2CO3 (飽和) + H2O + CO2 → 2NaHCO3
- フッ化水素 (希釈) との反応
Na2CO3 + 2HF→ 2NaF + H2O + CO2
- 空気にさらされた場合:
NaCO3•10H2O→Na2CO3•H2O+9H2O
したがって、炭酸ソーダは空気に触れると減量します。
- 暖房効果
NaCO3•10H2O→Na2CO3•H2O+9H2O
375K で
NaCO3•10H2O→Na2CO3+H2O
375K 以上
炭酸ナトリウム構造
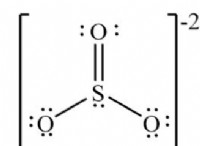
炭酸ナトリウムの各分子は、2 つのナトリウム原子、1 つの炭素原子、および 3 つの酸素原子で構成されています。解離すると、2 つのナトリウム カチオン (Na+) と 1 つの炭酸アニオン (CO3-2) を生成するイオン化合物です。
反応式
H2CO3 (炭酸) は弱酸ですが、2NaOH (水酸化ナトリウム) は強塩基です。したがって、炭酸ナトリウム (Na2CO3) は、弱酸と強塩基から引き出されます。炭酸ナトリウムは塩基性塩です。
H2CO3 + 2NaOH → Na2CO3 + 2H2O
結論
炭酸ナトリウムは、ソーダ灰として知られる有機化合物です。炭酸ナトリウムは、日常生活やさまざまな工業製品の製造においてさまざまな用途があります。希塩酸との反応や沸点、融点などの物理的および化学的特性があります。炭酸ナトリウムは、ホウ砂、リン酸ナトリウム、水ガラス、および他の多くのナトリウム化合物を作るために使用されます.それはしばしば洗濯ソーダと呼ばれ、すべての基本的な重化学物質の中で最も重要です. 炭酸ナトリウムは水に溶けます。 水酸化ナトリウムに対する炭酸ナトリウムの大きな利点は、炭酸ナトリウムが非腐食性であることです。したがって、取り扱いがより安全です。