はじめに
水素
構造
水素原子の構造は、静電力によって結合された 1 つの陽子と 1 つの電子で構成されています。最も外側の殻に 1 つの電子で構成されているため、電子を失うことも電子を獲得することも同じように簡単で、希ガス構成を達成できます。
資質
水素の原子番号は 1 で、文字 H で表されます。その核量は 1.0079 で、+1 と -1 の 2 つの酸化状態があります。それは非金属であり、酸素で燃焼して形成されます。ギリシャ語では、水のメーカーとして知られています。その低い融点と沸点は非常に低いです。無色、無臭、無味、可燃性の透明なガスで、自然界では二原子の形で存在します。
プロチウム、重水素、トリチウムと呼ばれる 3 つの同位体が知られています。しかし、3つの同位体の物理的性質には大きな違いがあります。初期の大宇宙では、陽子、水素原子核がビッグバン後の最初の1秒間に出現したと言われています。しかし、大宇宙全体で中性水素原子が出現したのは、約 370,000 年後の再結合時代で、電子が陽子に結合したままになるのに十分なほどプラズマが冷却されたときです。
宇宙の豊かさ
水素は、宇宙にかなり豊富に存在する化学元素です。しかし、宇宙の質量のほとんどは化学元素ではなく、暗黒物質や暗黒エネルギーなどのまだ検出されていない形態として実体化すると仮定されています。水素は恒星や巨大ガス惑星に過剰に存在します。水素の分子雲は、しばしば星の建設に関連しています。水素は、陽子-陽子反応を通じて星に電力を供給する上で重要な役割を果たします。
大宇宙全体を通して、水素は主に原子およびプラズマ状態で見られ、水素分子の特性とは幾分区別できる特性を持っています。プラズマの形では、水素の電子と陽子は同時に結合していません。その結果、非常に高い電気伝導率と高い光子放射率を持ち、太陽や他の星からの光を生成します.水素は、原子がぶつかったり混ざったりすることはめったにないため、星間媒体の中性原子状態で発見されます.地球上の通常の状況では、水素元素二原子気体として存在します。水素ガスは、重量が軽いため、重いガスよりも速く大気から逃げることができるため、地球の大気中にはほとんど存在しません。プロトン化水素分子と呼ばれる分子構造が星間物質で発見されました。これは、天体の光線からの分子水素の電離によって開発されました。木星の上層大気でも観測されています。このイオンは、宇宙空間の温度と密度が低いため、地球よりも宇宙空間で比較的安定しています。
重要性
私たちの日常生活における水素の重要な用途のいくつかは、
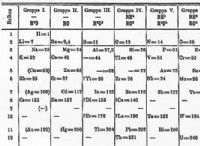
<オール>周期表における従来の位置
従来、水素は周期表のアルカリ金属の上に配置されていました。周期表の最初の行のナトリウム (Na) のすぐ上に位置しています。
理由
アルカリ金属との水素の位置付けは、主にその電子配置によるものです。水素原子は配置 1s1 を持ち、規則に従って配置される最初の要素である必要があります。もう1つの理由は、アルカリ金属のようにH +を形成するために電子の1つを失う可能性があることです.アルカリ金属と同様に1+1価の酸化状態を示します。非金属および還元性との反応は、アルカリ金属に似ています。
周期表における実行可能な位置
周期表における水素の通常の位置とは別に、別の実行可能な位置があります。これは、水素が物理的および化学的に多くの類似した特性を持ち、ハロゲンの中に配置されるためです.
理由
ハロゲンと同様に、水素も非常に高いイオン化エンタルピーを持ち、通常の条件下では非金属特性を持ちます。イオン化エンタルピーのおかげで、水素はアルカリ金属よりもハロゲンに似ていることが観察されます。また、ハロゲンに似た二原子分子として存在します(単一の水素結合を持っています)。金属と結合すると、陰イオンとして機能し、希ガス構成を達成するために 1 つの電子を必要とします。
結論
周期表における水素の位置のこの異常は、巨大で独自の化合物の世界を振り返る余地を与えてくれます。それらを分類しようとする試みは、単に便宜上のものです。すべての要素を正当な位置に置くことはできません。なぜなら、要素はグループではなく、独自に判断および研究されることを意図していたからです.