電子を軌道に入れる規則 – アウフバウの原理
はじめに
アウフバウの原理 は、ドイツの Aufbauprinzip (構築原理) から派生したもので、Aufbau 規則としても知られています。電子は、原子またはイオンのアクセス可能なエネルギー サブシェルの基底状態で最初に最も低く、次に高エネルギー サブシェルを占めると主張しています。たとえば、リン原子は 1s2 2s2 2p6 3s2 3p3 の配置を持ち、1s サブシェルが 2 つの電子を持っていることを示します。
フントの法則やパウリの排他原理など、他の原子物理学の原理は、電子の振る舞いを説明するのに役立ちます。フントの法則によると、同じエネルギーの多くの軌道にアクセスできる場合、電子はいずれかが 2 回占有される前に、個別の軌道を単独で占有します。二重占有が発生した場合、パウリの排他原理により、同じ軌道にある電子は異なるスピン (+½ と -1/2) を持つことが決まります。
ある元素から原子番号の大きい次の元素に移動するとき、その都度中性原子に 1 つの陽子と 1 つの電子が追加されます。どのシェルも、最大 2n 個の電子を持つことができます。ここで、n は一次量子数です。 2(2l + 1) は、サブシェル (s、p、d、または f) 内の電子の最大数です。ここで、l =0、1、2、3… 結果として、これらのサブシェルはそれぞれ最大 2 個を持つことができます。 、6、10、または 14 個の電子。合計数が原子番号に等しくなるまで、アクセス可能な最も低いサブシェルに電子を追加することにより、基底状態で電子配置を構築できます。その結果、サブシェルは、電子配置の予測に役立つ 2 つの広範な基準に基づいて、エネルギーが増加する順に充填されます。
- サブシェルは、n + l の値が大きい順に電子に割り当てられます。
- 2 つのサブシェルが同じ場合
n + l の値で、電子は下位の n からサブシェルに割り当てられます。
アウフバウ原理の変形である核殻モデル 、原子核内の陽子と中性子の配置を予測します。
Aufbau Principle Order :
アウフバウの原理は、エネルギーの高い軌道ほど実効核電荷が低いという仮定に基づいています。軌道上の電子は、負電荷の雲のように振る舞います。電子が多ければ多いほど、雲はより負になります。そのため、電子が低エネルギーの軌道に落ちると、有効な核電荷が減少し、残りの軌道に他の電子が引き寄せられます。 Aufbau は、電子を軌道に入れる規則について多くの重要なことを述べています。 .
まとめると、これら 2 つの原則は、特定の原子が特定の軌道に複数の電子を持つことは決してないことを意味します。これは、ボーアの仮説を説明しています。電子は、エネルギーが増加する順に軌道を満たし、1 軌道あたり 1 つの電子であり、例外はありません。
アウフバウ原理またはアウフバウ列とも呼ばれる (n+l) 規則は、すべての原子軌道のエネルギーを決定します。このルールは、(n+l) の値が小さい軌道が最初に満たされることを示しています。 2 つの軌道の n+l が同じ場合、n が小さい軌道が先に埋められます。
最初に入力する軌道は 1s 軌道です。これは2つの電子で満たされます。 2s 軌道を埋める次の軌道。それは別の2つの電子で満たされます。 3 番目に満たされる軌道は 2p 軌道で、さらに 6 個の電子で満たされます。次に埋める軌道は 3s 軌道と 3p 軌道で、それぞれさらに 8 個の電子で満たされます。
次に高いエネルギー準位には 4 つの軌道があります。次のようにそれらを埋めます。4s は 2 つの電子で埋められます。 4p は 6 でいっぱいになります。そして、10 個の電子で満たされる 4d が来ます。それに続くのは、8個の電子で満たされた5sです。次に5dが来て、さらに14でいっぱいになります。そして最後に 5p の充填が行われます。これにより、さらに 18 個の電子が充填されて、充填された軌道グループのリストが完成します。
したがって、次の図は、軌道の充填をよりよく視覚化するために使用できます。

矢印の尾から頭に移動し、下の矢印の尾に移動します。
この順序でそれらを書き留めると、軌道エネルギーの昇順と、電子が原子に満たされる順序がわかります。
例外:
クロムの電子配置は [Ar]3d54s1 であり、[Ar]3d44s2 ではありません (アウフバウの原理で示唆されています) )。これは、半充填サブシェルの強化された安定性や、3d と 4s サブシェル間の比較的小さなエネルギー ギャップなど、いくつかの変数によるものです。
半分満たされたサブシェルの軌道での電子間反発が低いと、電子間反発が減り、安定性が向上します。同様に、満たされたサブシェルは原子の安定性を向上させます。その結果、一部の原子の電子配置は Aufbau に逆らいます。 原則 (軌道間のエネルギーギャップによる)。
たとえば、銅はこのルールの例外であり、[Ar]3d104s1 に対応する電気的配置を持っています。充填された 3D サブシェルによって得られる安定性がこれを説明しています。
さまざまな軌道に電子を充填するためのルール:
<オール>フントの法則は次のとおりです。
- サブレベルの軌道が 2 重占有される前に、1 重占有されます。
- 単一占有軌道内のすべての電子は、全体のスピンを最大化するために同じスピンを持っています。
電子は、すべての軌道を同様のエネルギーで満たすことができるため、半分満たされた軌道で別の電子と結合しません。基底状態の原子には、多数の不対電子があります。 2 つの電子が接触すると、2 つの磁石と同じように振る舞います。対になる前に、電子は互いにできるだけ離れたいと考えています。
<オール>結論
アウフバウの原則 電子デバイスの構成に使用されます:
- 執筆中の硫黄電子配置
- 硫黄の原子番号は 16 で、16 個の電子があることを示しています。
- アウフバウの原則による 、これらの電子のうち 2 つは 1s サブシェルにあり、8 個は 2s および 2p サブシェルにあり、残りは 3s および 3p サブシェルの間に分散しています。
その結果、硫黄の電子配置は 1s22s22p63s23p4 と表すことができます。
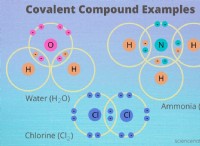
窒素電子配置 :
- 窒素は 7 電子元素です (原子番号が 7 であるため)。
- 電子は 1s、2s、および 2p 軌道を占有します。
- 窒素の電子配置は 1s22s22p3 と表記されます。