主な違い – 求核置換反応と求電子置換反応
求核置換反応と求電子置換反応の両方が、有機化学と無機化学で見られます。これらの置換反応は、特定の化合物の合成において非常に重要です。置換反応は、別の原子または原子団による原子または原子団の置換を含む反応です。求核置換反応と求電子置換反応の主な違いは、求核置換反応には求核剤による脱離基の置換が含まれるのに対し、求電子置換反応には求電子剤による官能基の置換が含まれることです。
対象となる主な分野
1. 求核置換反応とは
– 定義、反応過程、例
2. 求電子置換反応とは
– 定義、反応過程、例
3. 求核置換反応と求電子置換反応の違い
– 主な違いの比較
重要な用語:脂肪族および芳香族化合物、求電子試薬、求電子置換、脱離基、求核試薬、求核置換、SE 1 件の反応、 SE 2 リアクション、SN 1 件の反応、 SN 2 反応、 置換反応 
求核置換反応とは
求核置換反応は、求核剤による脱離基の置換を伴う化学反応です。この脱離基は、求核剤が脱離基が結合している分子と反応すると脱離するため、その名前が付けられています(分子全体を基質と呼びます)。求核剤がくっつく部分を求電子剤と呼びます。この求電子剤は、安定するために電子を欠いています。したがって、求核試薬から電子を受け取ります。これにより、求核剤と求電子剤の間に共有結合が形成されます。
ほとんどの場合、求核試薬は負に帯電しています。しかし、それは、すぐに供与される自由な電子対を持つ中性荷電分子である可能性もあります。これらの求核置換反応は、脂肪族および芳香族有機化合物で起こります。
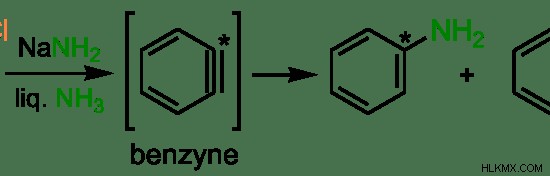
図 1:芳香族化合物における求核置換の例
上の例では、ベンゼン環が塩素 (Cl) 原子に結合しています。 NaNH2存在下での脱離基です。 .求核試薬は –NH2 グループ。炭素原子 (上の画像の星印) は求核試薬によって攻撃され、Cl 原子は –NH2 によって置換されます。 グループ。これは求核置換と呼ばれます。
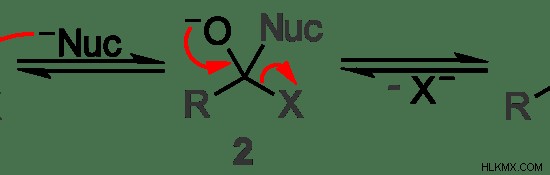
図 2:芳香族化合物における求核置換の例
上記の例では、求核試薬は記号「Nuc」で示されています。中心の炭素原子は求核剤によって攻撃され、脱離基「X」は求核剤によって置換されます。上の画像の最初の分子と最後の分子の違いを考えると、はっきりとわかります。
メカニズムに従って分類される求核置換反応には、主に 2 つのタイプがあります。
SN 1 リアクション
記号「S」は「置換」を表し、「N」は「求核性」を表します。数字(ここでは「1」)は、反応の速度論的順序を示します。これらの反応には、カルボカチオン中間体の形成が含まれます。したがって、反応は 2 段階で発生します。
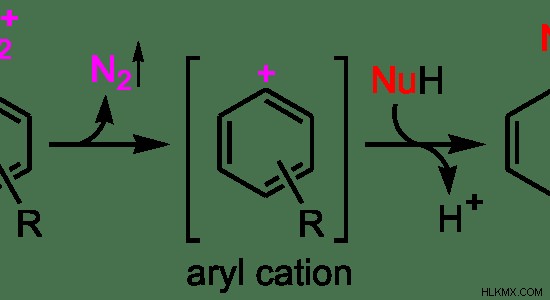
図 3:SN1 の反応メカニズム
上の例では、N2 は最初の分子の脱離基です。最初のステップとして、脱離基が脱離し、カルボカチオン中間体が形成されます。ここで形成される中間体はアリールカチオンです。それは安定したイオンであるため、これがこの反応の律速段階です。 2 番目のステップとして、求核剤がカルボカチオンに結合します。
SN 2 リアクション
SN 2 反応では、カルボカチオンは形成されません。したがって、反応は単一のステップで発生します。したがって、これは反応の律速段階です。
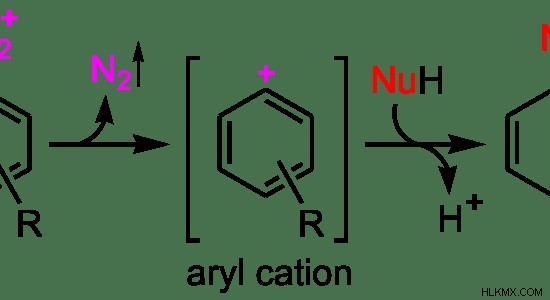
図 4:SN2 反応メカニズム
上記の例は、脱離基 (ここでは「X」) の脱離と求核剤の置換が同時に起こっていることを示しています。続きを読む:SN の違い 1 と SN 2 リアクション。
求電子置換反応とは
求電子置換は、求電子剤による官能基の置換を伴う化学反応です。ほとんどの場合、水素原子はこのように置換されます。求電子置換反応は、脂肪族および芳香族化合物にも見られます。求電子置換反応は、特にベンゼン誘導体の作成に使用されます。
求電子剤は、正または中性に帯電しているが電子を欠いている分子です。求電子剤は、その電荷を中和するため、またはオクテット規則に従って安定するために、求核剤から電子を受け取ります。
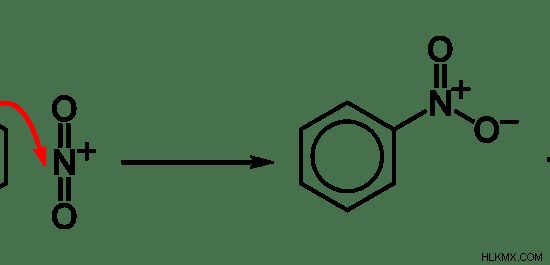
図 5:芳香族化合物における求電子置換反応の例
上記の例では、ベンゼン環の 1 つの水素原子が NO2 に置換されています。 イオン。この場合、NO2 求電子剤です。窒素原子には正電荷があります。ベンゼン環は、パイ結合の存在により電子が豊富です。したがって、求電子剤はベンゼン環を攻撃して結合し、水素原子を「脱離基」にします。
求電子置換反応は、主に 2 種類のメカニズムで見られます。
SE 1 リアクション
これらの SE 1 反応には、安定したカルボカチオンの形成が含まれます。したがって、律速段階はカルボカチオン形成の段階である。これは、SE 1 反応は 2 段階で起こります。カルボカチオンへの求電子剤の付着もここで観察できます。しかし、脱離基は依然としてカルボカチオンに結合しています。第二段階として、脱退組の脱退が発生する。

図 6:SE1 反応メカニズム
SE 2 リアクション
SE 2 反応は 1 ステップのみです。カルボカチオンは形成されません。したがって、律速段階は置換分子の形成です。
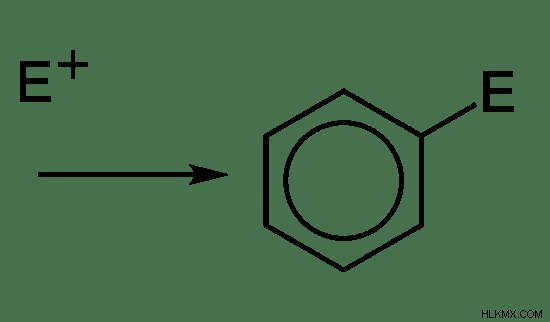
図 7:SE2 反応メカニズム
求核置換反応と求電子置換反応の類似点
-
どちらのタイプの反応も電子共有に関連しています。
-
どちらの反応も共有結合になります。
-
どちらの反応も、基質分子に存在する基の置換をもたらします。
-
彼らは脱退グループを生み出します。
-
どちらのタイプの反応も、脂肪族および芳香族化合物に関連する化学反応に見られます。
求核置換反応と求電子置換反応の違い
定義
求核置換反応: 求核置換反応は、求核試薬による脱離基の置換を伴う化学反応です。
求電子置換反応: 求電子置換は、求電子剤による官能基の置換を伴う化学反応です。
電子共有
求核置換反応: 求核置換反応では、求核剤がその電子を供与します。
求電子置換反応: 求電子置換反応では、求電子剤が電子を受け取ります。
電荷
求核置換反応: 求核置換反応では、求核剤は負または中性に帯電し、電子受容分子は正または中性に帯電します。
求電子置換反応: 求電子置換反応では、求電子剤は正または中性に帯電し、電子供与分子は負または中性に帯電します。
結論
求核および求電子置換反応は、有機および無機化学における基本的な反応です。求核置換反応と求電子置換反応の主な違いは、求核置換反応には求核試薬による脱離基の置換が含まれるのに対し、求電子置換反応には求電子試薬による官能基の置換が含まれることです。
画像提供:
1. コモンズ ウィキメディア経由の「ベンザインによる置換」(パブリック ドメイン)
2. Ckalnmalsによる「塩基触媒求核アシル置換の一般的なスキーム」–コモンズウィキメディア経由の自作(CC BY-SA 3.0)
3. 「ベンゼンニトロ化メカニズム」Benjah-bmm27 著 – Commons Wikimedia 経由の自身の作品 (パブリック ドメイン)
4. 「芳香族 SN1 メカニズム」(パブリック ドメイン) Commons Wikimedia 経由
5. 「Mechanismus der Sn2 Reaktion-Seite001」Poyraz 72 著 – Commons Wikimedia 経由の自作 (CC BY-SA 3.0)
6.コモンズ ウィキメディア経由の「アレニウム イオン メカニズム」(パブリック ドメイン)
参照:
1.」求電子置換。」求電子置換とは何ですか? N.p.、n.d.ウェブ。こちらから入手できます。 2017 年 6 月 27 日.
2.Hunt、Dr Ian R.「求核置換」。 Ch 8:求核置換。 N.p.、n.d.ウェブ。こちらから入手できます。 2017 年 6 月 27 日.
3."B.求核置換とは?」化学LibreTexts。 Libretexts、2016 年 6 月 24 日。ウェブ。こちらから入手できます。 2017 年 6 月 27 日