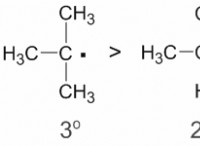
誘導効果とは、分子内の結合電子の不均等な共有による永久双極子の形成を意味します。この効果はシグマ結合で発生する可能性がありますが、エレクトロマー効果はパイ結合で発生する可能性があります。この記事では、誘導効果を持つ化合物の酸性度または塩基性度の測定について説明します。
分子の酸性度と塩基性度に対する誘導効果の影響
誘導効果を使用して、錯体の酸性度と塩基性度を推定できます。一般に、電子吸引基 (EWG) は複合体の酸性度を高め、電子供与基 (EDG) は化合物の酸性度を低下させます。
- これは、R が電子求引性である場合、酸の共役塩基である RCOO– が、形成された負電荷の非局在化によって安定化されるためです。
- R が電子を供与した場合、共役塩基は電子間反発によって不安定になります。
- したがって、+I 効果は酸度を下げ、-I 効果は酸度を上げます。
- たとえば、ギ酸は、カルボキシル基に結合したメチル基の +I 誘導効果を受け継ぐため、酢酸 (CH3COOH) よりも酸性です。
誘導効果の種類
-I 効果
粒子またはグループが結合電子を引き寄せ、部分的に負電荷を得る場合、それは -I グループと呼ばれ、関連する効果は電子吸引誘導効果または -I 効果と呼ばれます。
+I 効果
粒子またはグループが結合に電子を供与し、部分的に正電荷を獲得する場合、それは +I グループと呼ばれ、関連する効果は正の誘導効果または +I 効果と呼ばれます。
誘導効果のある化合物の酸性度または塩基性度の測定 (解決例) の質問
質問 1: フルオロ酢酸とクロロ酢酸のうち、酸性度が高いのはどれ?
解決策: フッ素と塩素の電気陰性度はそれぞれ4.1と2.8なので、フルオロ酢酸の方が強いと予想されます。これら 2 つの酸の pKa 値は、それぞれ 2.39 と 2.68 です。確かに、フルオロ酢酸の方が強いですが、その差は大きくありません.
質問 2: アミンの比較塩基強度は、__________ の影響を受けません。
<オール>解決策: 正解はbです。アミンの相対的な塩基強度は、メソメリック効果に依存しません。この効果は定性的に使用され、関連する共鳴構造に基づいて置換基の電子吸引または放出特性を表します。
質問 3:
以下のグループを -I 効果の減少に従って並べ替えます。
- CN> F> Br> Cl> COOH> I> H
- CN> COOH> F> Cl> Br> I> H
- H> COOH> CN> I> Cl> F> Cl
- COOH> CN> F> Br> Cl> I> H
- これらのどれでもない
解決策: 選択肢bが正解です。

誘導効果と電荷の非局在化は、化合物の酸性度または塩基性度に大きな影響を与えます。分子の酸塩基強度は、その構造に大きく影響されます。
A–H または B–H+ 結合が弱い場合、H+ イオンに解離する可能性が高くなります。さらに、H + の解離を促進する要因は、共役塩基上に存在する孤立電子対の安定性を促進し、共役酸をより強い酸にします。
原子や原子団などの分子の一部は、誘導効果を通じて酸または塩基の強度に影響を与える役割を果たします。これにより、O–H 結合の強度が低下し、水素が H+ イオンとしてより簡単に解放されます。
結論
この記事では、誘導効果を持つ化合物の酸性度または塩基性度の測定について説明します。誘導効果は、σ電子の結合が結合の電気陰性要素に向かって部分的にシフトすることです。この効果はシグマ結合で発生する可能性がありますが、エレクトロマー効果はパイ結合で発生する可能性があります。この記事では、解決済みの例を使用して、誘導効果を持つ化合物の酸性度または塩基性度を測定することを研究しました.