化学反応は、反応物とは異なる独自の物質を形成するために起こります。世界中のあらゆるメカニズムが、反応の反応物を組み合わせることによって生成物を生成します。食品の準備と消化から燃料の形成まで、化学反応は重要な役割を果たします。化学反応の方向を予測するために平衡定数を使用します。反応にガスが含まれる場合、式は蒸気密度測定値から得られます。
化学反応
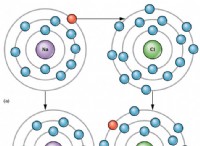
- 化学反応とは、2 つ以上の化学物質 (反応物) が相互作用して 1 つ以上の生成物を形成する一連のプロセスです。
- 一般に、化学反応には 2 つの側面があります。
- 左側には反応物が含まれています。右側には、反応物間の反応によって形成された生成物があります。
- 記号形式の化学反応は、A + B → C + D として表されます。
リアクションの方向
化学反応の方向は、反応がどのように起こっているかです。化学反応は、不可逆反応と可逆反応の 2 つに分類されます。
不可逆反応
- 不可逆反応では、反応物が生成物を形成します。
- このような反応は、反応物を生成する製品のように可逆的ではありません。
- 不可逆的な化学反応の一般的な表現は、A + B → C + D
たとえば、
C + O2 → CO2 [炭素 + 酸素 → 二酸化炭素]
可逆反応
- 可逆反応では、反応物が生成物を形成し、生成物が反応して反応物を生成します。
- これは双方向であり、双方向で行われます。
- 可逆的な化学反応の一般的な表現は、A + B ⇄ C + D です。
たとえば、
N2 + O2 ⇄ 2NO [窒素 + 酸素 ⇄ 2 亜酸化窒素]
- 反応に関与する元素は気体です。
- したがって、反応の方向は蒸気密度測定から予測できます。
反応の方向を予測するための平衡定数
化学反応の平衡は、反応物と生成物がそれ以上相互作用しない状態です。反応が残っています。可逆反応のこの段階では、質量作用の法則に従って、反応物の濃度が生成物の濃度と等しくなります。
平衡定数の計算方法
化学反応では、aA + bB ⇄ cC + dD ここで、
- A と B は反応物です。 a と b は、それぞれの化学量論数です。
- C と D は製品です。 c と d は、それぞれの化学量論数です。
平衡定数 Kc は次のように計算されます
K
平衡定数は、反応物の濃度に対する生成物の濃度の比率です。ここで、化学反応は平衡状態にあります。
反応指数の計算方法
化学反応では、aA + bB ⇄ cC + dD ここで、
- A と B は反応物です。 a と b は、それぞれの化学量論数です。
- C と D は製品です。 c と d は、それぞれの化学量論数です。
反応商 Qc は次のように計算されます
Qc =[C] [D] /[A] [B]
反応商は、反応が平衡状態にないことを除いて、平衡定数と同じです。
反応の方向を予測する
化学反応の平衡定数と反応商の値を知ることにより、反応の方向を予測することができます。反応物と生成物が気体の場合、方向は気体の蒸気密度測定から得られます。反応の方向を予測する 3 つの異なる条件は次のとおりです。
逆反応
Qc> Kc
Qc の値が Kc の値より大きい場合、
- 反応が逆方向に進んでいます。
- 生成物が反応して反応物を形成していることを意味します。
- 反応の方向は右側から左側です。
- 反応が逆方向に進んでいます。
前向きな反応
Qc
Qc の値が Kc の値より小さい場合、
Qc =Kc
Qc の値が Kc の値と同じ場合、
化学反応は、不可逆的または可逆的である可能性があります。可逆反応では、反応の方向を決定するために特定のパラメーターが考慮されます。反応の方向を予測するために平衡定数を使用することとは別に、反応商の値も重要な役割を果たします。化学反応商が平衡定数よりも大きい場合、反応は逆方向になります。平衡定数が大きいほど、化学反応は進行します。両方の値が等しい場合、反応は停止します。
平衡反応
結論