室温では、ジボランは無色の気体で、不快な甘い香りがします。空気と混合すると、爆発的な組み合わせを簡単に生成できます。室温では、ジボランは湿った空気中で自然発火します。ジボランは、還元剤、ゴム加硫剤、炭化水素重合の触媒、火炎速度促進剤、ロケット推進薬のドーピング剤として使用されます。また、純粋な水晶の電気的特性を与えるためにエレクトロニクスでも使用されます。
水はジボランを分解し、揮発性ガスである水素ガスと制御されていない物質であるホウ酸を放出します。その蒸気は空気より重い。低レベルへの長期暴露または高濃度への短期暴露の後、これらの蒸気を吸入すると、健康に悪影響を与える可能性があります。電子材料にも使用されています。
ジボランについて
ジボランの調製
金属水素化物とホウ素の作用でジボランを作ることができます。このプロセスは、工業生産に使用されます。ヨウ素を水素化ホウ素ナトリウムと反応させて少量のジボランを得るには、ジグリムが必要です。

プロパティ
ボランは、本質的に無色で、熱安定性が低い反磁性化合物です。ジボランは甘い香りのガスで、室温では非常に有毒です。反応性も高いです。高温でより多くのボランを生成し、水素を放出します。
ジボランは水とアルカリと反応して、ホウ酸とメタボレートを生成します。

ハイドロボレーション
室温では、ジボランはエーテル溶媒中でアルケンおよびアルキンと結合します。ヒドロホウ素化は、特に反マルコフニコフ付加のために、有機合成化学で一般的に使用される反応です。

空気の作用
純粋なジボランは室温で空気や酸素と反応しませんが、不純な形では大量の熱とともに B2O3 を生成します。

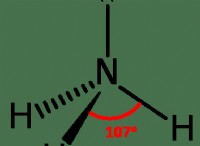
ジボランの構造
2 つの架橋水素は、ジボランの 2 つの BH2 ユニットを接続します。したがって、8つのB-H結合が含まれています。一方、ジボランには 12 個の価電子しかなく、通常の共有結合を作成するには不十分です。通常の共有結合は、4 末端 B-H 結合 (2 つの中心 - 2 電子結合または 2c-2e 結合) を構成します。架橋結合には、残りの 4 つの電子が必要です。 2 つの 3 中心 B-H-B 結合のそれぞれで 2 つの電子が使用されます。その結果、これらは 3 中心 2 電子結合 (3c-2e) になります。ジボランのホウ素はsp3混成です。
4 つの sp3 混成軌道のうち 3 つは単一の電子を含み、4 番目の軌道は空です。各ホウ素には、2 つの水素とオーバーラップして 4 末端 2c-2e 結合を生成する 2 つの半充填混成軌道があり、1 つの空と 1 つの半充填混成軌道が残ります。 B-H-B 結合は、1 つのホウ素の半分満たされた混成軌道、もう 1 つのホウ素の空の混成軌道、および水素の半分満たされた 1s 軌道を重ねることによって形成されます。
絆
ジボランは、4 つの末端水素原子と 2 つの架橋水素原子を持つ D2h 構造を持っています。分子軌道理論モデルによると、ホウ素と末端水素原子の間のリンクは、標準的な 2 中心 2 電子共有結合です。ただし、炭化水素化合物とは対照的に、ホウ素原子と架橋水素原子の関係は異なります。
各ホウ素は、末端の水素原子に 2 つの電子で結合した後、さらに結合するために 1 つの価電子を残しています。架橋水素原子のそれぞれが 1 つの電子に寄与します。その結果、4 個の電子が B2H2 リングを一緒に保持します。これは、3 中心 2 電子結合の例です。この形の絆は「バナナ絆」と呼ばれることもあります。
絆
ジボランとその誘導体は、B-H 結合にアルケンを付加してトリアルキル ボランを生成するヒドロホウ素化の重要な有機合成試薬です。ジボランは、水素化アルミニウムリチウムと同様の反応性を持つ還元剤として利用されます。この分子はカルボン酸をアルコールに素早く変換しますが、ケトンは出発物質の酸とゆっくりとしか反応しません。
ジボランの用途
<オール>結論
最も典型的な反応パターンの 1 つは、ルイス塩基との付加物の形成です。このような最初の付加物は、他の製品を生成するために頻繁に迅速に開発されます。たとえば、ボラン-テトラヒドロフランは、ジボランの代替として一般的に使用されるボレートエステルに分解されます。その硫化ジメチル付加物は重要な化学試薬です。アンモニアジボランはアンモニアボランと結合して、条件に応じてジボランのジアモニエートまたは DADB を生成します。