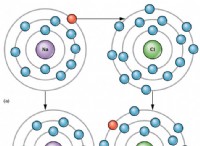
化学反応とは、反応物と呼ばれる他の元素と反応して新しい化学物質を形成するプロセス、または元素を組み合わせて新しい物質を形成するプロセスと言えます。化学反応には二つの要素があり、一つは互いに反応して化学変化する「反応物質」と、その反応の結果生成される「生成物」です。化学反応の例の 1 つは、Na と Cl が互いに反応して生成される NaCl の生成です。
- 互いに反応して新しい元素を生成するための 2 つの化合物の融合
- 化学反応は通常、元素の化学的性質を変化させます。
- 化学反応中には、色の変化、沈殿物の形成、熱や火の発生など、いくつかの物理的変化も観察されています。
- 原子間に存在する結合は化学反応中に分解され、可逆的または不可逆的なまったく新しい化合物を形成します。
- 反応速度は常に、元素の性質、結合の強さ、および温度、圧力、光などの外部要因によって異なります。
- 身体的変化
- 化学変化
さまざまな変更点の説明:
| 化学変化 | 身体の変化 |
| 異なる化学的性質を持つ新しい物質が形成される化学反応の後、その変化は化学変化と呼ばれます | そのような要素の生成が発生しなかった場合、その変化は物理的変化と呼ばれます。 |
| 例:紙を燃やした後、元の状態に戻せない炭素が生成されます。 | 例:氷が溶けて水になり、物理的性質は変化しますが、化学的性質は変わりません。 |
X + Y → P + Q上記の反応では、X と Y は反応成分であり、P と Q は反応の生成物です。化学反応の種類:異なる化学物質または物理的な文字。また、反応の種類は、反応物質の性質と反応に必要な要因によって異なります。
燃焼反応:酸化剤と燃料との反応により、火が発生し、温度が上昇し、大量の熱と酸化還元化学物質を生成する反応は、燃焼反応と呼ばれます。
酸素は、燃焼反応の主要なケースで主要な酸化剤として機能します。燃焼反応には 2 つのタイプがあります。
- 燃料が完全燃焼したら完全燃焼
- 酸化剤の存在が限られているために燃料が部分的に燃焼する場合の不完全燃焼
私たちの体内のブドウ糖は、酸素の存在下でエネルギーを持って二酸化炭素と水に酸化されます。
C6 H12 O6 + 6O2 → 6CO2 + 6H2 O+エネルギー
化学分解反応:分解は、光や熱などの外部要因の影響により、1 つの成分が 2 つ以上の成分に分解されるプロセスです。このプロセスでは、1 つの反応物が 2 つ以上の単純な生成物に分解されます。
化学分解反応は3種類 -
- 熱エネルギーの影響で反応する熱分解
- 電気エネルギーの作用によって起こる電解分解
- 光子の吸収によって起こる光分解
熱または熱エネルギーの影響により、炭酸カルシウムは酸化カルシウムと二酸化炭素に分解されます。熱分解の一種です。
CaCO3 →CaO + CO2
中和反応:中和反応は、副産物として塩と水を形成する酸性化合物と塩基性化合物との間の反応プロセスです。 H+ と OH- イオンが結合して水 (H2 O)。基本的には「酸塩基中和」反応です。
例:
酸 HCl と塩基 NaOH との反応による塩化ナトリウムの形成。
HCl + NaOH → NaCl + H2 〇
レドックス反応:基本的には、反応物間で電子を移動させる還元 - 酸化反応です。
例:Mg は酸化されて酸化マグネシウムを生成しますが、MgO は酸素で還元されます。
2Mg + O2 →2MgO
合成反応:合成反応は、まったく異なる生成物分子を生成する 2 つの異なる原子または物質間の反応の発熱プロセスです。例:ナトリウムと塩素が互いに反応して、塩化ナトリウムと呼ばれる一般的な塩を形成します。
2Na + Cl2 →2NaCl