主な違い – EDTA 二ナトリウムと EDTA 四ナトリウム
EDTA はよく知られているキレート剤です。カルシウムやマグネシウムなどの金属イオンと結合することができます。 EDTA は金属イオンの「隔離」を引き起こします。これは、金属イオンと結合し、安定した EDTA-金属錯体を形成することによって行われます。 EDTA 二ナトリウムと EDTA 四ナトリウムは、多くの業界で使用されている 2 つの形態の EDTA です。それらはEDTAのナトリウム塩です。 EDTA 二ナトリウムには 2 つのナトリウム カチオンがありますが、EDTA 四ナトリウムには 1 分子あたり 4 つのナトリウム カチオンがあります。 EDTA 二ナトリウムと EDTA 四ナトリウムの主な違いは、EDTA 二ナトリウムの pH が 7 より低いのに対し、EDTA 四ナトリウムの pH は 7 より高いことです。
対象となる主な分野
1. EDTA二ナトリウムとは
– 定義、構造、用途
2. EDTA四ナトリウムとは
– 定義、構造、用途
3. EDTA二ナトリウムとEDTA四ナトリウムの類似点は何ですか
– 共通機能の概要
4. EDTA二ナトリウムとEDTA四ナトリウムの違いは何ですか
– 主な相違点の比較
主な用語:EDTA 二ナトリウム、EDTA、エデト酸二ナトリウム、陽イオン ナトリウム、EDTA 四ナトリウム 
EDTA二ナトリウムとは
EDTA 二ナトリウムは、2 つのナトリウム カチオンから構成される EDTA の一種です。 EDTA は一般に、その構造内に 4 つの負に帯電した酸素原子を持っています。二ナトリウム EDTA では、これらの酸素原子の 2 つが 2 つのナトリウム カチオンと結合しています。二ナトリウム EDTA は EDTA の合成の副産物です。 EDTA の合成には、エチレンジアミン、ホルムアルデヒド、およびシアン化ナトリウムが含まれます。したがって、EDTA 二ナトリウムに含まれるナトリウム イオンは、シアン化ナトリウムに由来します。
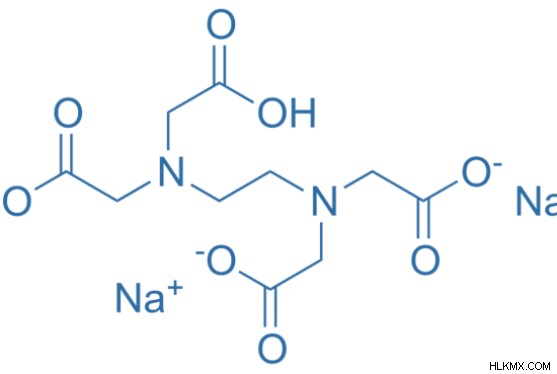
図 1:EDTA 二ナトリウムの化学構造
EDTA 二ナトリウムの分子式は C10 として与えられます H14 N2 ナ2 O8 .この化合物のモル質量は約 336.2 g/mol です。 EDTA 二ナトリウムはエデト酸二ナトリウムと呼ばれます 同じように。重金属キレート剤です。この化合物は、乾燥粉末または他の固体の形で入手できます。白色の結晶性粉末のように見えます。 EDTA 二ナトリウム溶液の pH は 4 から 6 の範囲ですが、7 を超えることはありません。
EDTA 二ナトリウムは、日常生活で使用するほとんどの製品に含まれています。例としては、シャンプー、染毛剤、ローション、シャワージェルなどがあります。製品の貯蔵寿命を延ばし、起泡性を高めるために化粧品に添加されます。医学における EDTA 二ナトリウムの役割には、キレート療法、抗凝固などが含まれます。それとは別に、この化合物は食品添加物としても使用されます。
しかし、ヒューマンケア製品に EDTA 二ナトリウムを使用することにはいくつかの危険性があります。これらの製品にはごく少量しか使用されていないため、有害な成分とは見なされていません。ただし、皮膚への浸透を促進するため、お客様は製品に含まれる他の成分にも注意する必要があります.
EDTA四ナトリウムとは
四ナトリウム EDTA は、4 つのナトリウム カチオンで構成される EDTA の一種です。 EDTA には 4 つの負に帯電した酸素原子があるため、これらの酸素原子はすべて EDTA 四ナトリウム化合物のナトリウム カチオンに結合しています。この化合物のモル質量は約 380.1 g/mol です。 EDTA 四ナトリウムの化学式は C10 です。 H14 N2 ナ4 O8 . EDTA 四ナトリウムは、EDTA 合成の副産物です。
EDTA 四ナトリウムは、乾燥粉末、液体などの形で入手できます。無色の結晶性粉末のように見えます。 EDTA四ナトリウムは水溶性です。エタノールにわずかに溶ける。 EDTA 四ナトリウム溶液の pH は 10 から 11 の範囲です。
EDTA 四ナトリウムの主な用途には、水軟化剤および防腐剤としての使用が含まれます。この化合物は、パーソナルケア製品や化粧品に使用されています。この成分は、金属イオンを封鎖する能力のために追加されています。この隔離により、EDTA 四ナトリウムが金属イオンと結合して、製品の他の成分との反応を防ぐことができるため、保存期間が長くなります。

図 2:EDTA 四ナトリウムは多くの化粧品の成分です
しかし、EDTA 四ナトリウムは、その使用法に応じて、低度から中程度の有害化合物と見なされます。その影響は、皮膚の炎症や毒性を引き起こす可能性があります。最も重要なことは、EDTA 四ナトリウムがエコトキシンとして認識されていることです (環境に有害です)。
EDTA二ナトリウムとEDTA四ナトリウムの類似点
- どちらの化合物も EDTA 合成プロセスの副産物です。
- どちらの化合物も EDTA のナトリウム塩です。
- どちらの化合物も水軟化剤および防腐剤として機能します。
- どちらの化合物も、パーソナルケア製品や化粧品の原料として使用されています。
EDTA二ナトリウムとEDTA四ナトリウムの違い
定義
EDTA二ナトリウム: 二ナトリウム EDTA は、2 つのナトリウム カチオンで構成される EDTA の一種です。
EDTA四ナトリウム: 四ナトリウム EDTA は、4 つのナトリウム カチオンで構成される EDTA の一種です。
化学式
EDTA二ナトリウム: EDTA二ナトリウムの化学式はC10 H14 N2 ナ2 O8 .
EDTA四ナトリウム: EDTA 四ナトリウムの化学式は C10 です。 H14 N2 ナ4 O8 .
モル質量
EDTA二ナトリウム: EDTA 二ナトリウムのモル質量は約 336.2 g/mol です。
EDTA四ナトリウム: EDTA 四ナトリウムのモル質量は約 380.1 g/mol です。
通常の pH
EDTA二ナトリウム: EDTA 二ナトリウム溶液の pH は 4 から 6 の範囲です。
EDTA四ナトリウム: EDTA 四ナトリウム溶液の pH は 10 から 11 の範囲です。
結論
EDTA 二ナトリウムと EDTA 四ナトリウムは、EDTA 合成プロセスの副産物です。それらはEDTAのナトリウム塩です。これらの化合物は、化粧品やその他のヒューマンケア製品の防腐剤として使用されています。 EDTA 二ナトリウムと EDTA 四ナトリウムの主な違いは、EDTA 二ナトリウムの pH が 7 より低いのに対し、EDTA 四ナトリウムの pH は 7 より高いことです。