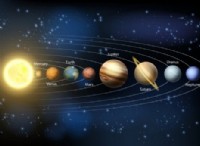
$$ ph =pk_a + log \ frac {[a^ - ]} {[ha]} $$
どこ:
* pHは溶液の酸性度です
* PKAは弱酸の酸解離定数です
* [a-]は、弱酸の共役ベースの濃度です
* [ha]は弱酸の濃度です
Henderson-Hasselbalch方程式を使用して、バッファー溶液のpHを計算できます。私たちは、私たちが作りたいバッファー溶液のpH(4.75)とベンゾ酸のPKA(4.20)を知っています。また、ベンゾ酸のコンジュゲートベースの濃度は、ベンゾ酸ナトリウムの濃度に等しいと仮定することもできます。したがって、ヘンダーソンハッセルバルチ方程式を再配置して、ベンゾ酸の濃度を解くことができます。
$$ [ha] =\ frac {[a^ - ]} {10^{ph -pk_a}} $$
私たちが知っている値を方程式に置き換えると、次のようになります。
$$ [ha] =\ frac {0.025} {10^{4.75-4.20}} =0.0040 m $$
バッファー溶液中のベンゾ酸とベンゾエートナトリウムの総濃度は0.029 Mです。したがって、500 mLの緩衝液を作るために追加する必要がある0.200 mベンゾ酸の体積は次のとおりです。
$$ v_ {ba} =\ frac {(0.0040 m)(500 ml)} {0.200 m} =10.0 ml $$
500 mLのバッファー溶液を作るために追加する必要がある2.00 mの水酸化ナトリウムの体積は次のとおりです。
$$ v_ {naoh} =\ frac {(0.025 m)(500 ml)} {2.00 m} =6.25 ml $$
したがって、10.0 mLの0.200 mベンゾ酸と6.25 mLの2.00 m水酸化ナトリウムを加えて、475ベンゾ酸25 NaOHで作られたものと同じpHを持つ500 mLのバッファー溶液を作る必要があります。