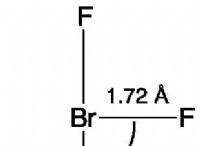
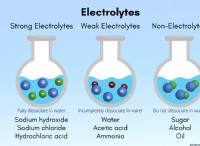
電解質溶液を形成する物質のいくつかの例は次のとおりです。
- 塩酸(HCl)や硫酸(H2SO4)などの酸
- 水酸化ナトリウム(NaOH)や水酸化カリウム(KOH)などの塩基
- 塩化ナトリウム(NaCl)や硝酸カリウム(KNO3)などの塩
これらの物質を水に溶解すると、構成イオンに分離します。たとえば、塩化ナトリウムを水に溶解すると、ナトリウムイオン(Na+)および塩化物イオン(Cl-)に分離します。これらのイオンは、溶液の周りを自由に移動し、電荷を持ち運びます。
電解質溶液は、神経伝達、筋肉収縮、心臓の機能など、多くの生物学的プロセスで役割を果たすため、重要です。また、バッテリー、電気めっき、水処理など、さまざまな産業用途でも使用されています。