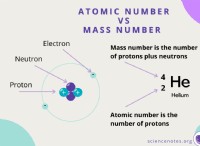
ルビジウム-85の場合、具体的には合計37電子があります。その中性状態では、その核内の正の帯電した陽子の数は、37の負に帯電した電子によってバランスが取れています。 1電荷のイオンになるには、1つの電子を失い、36個の電子と37個のプロトンを残す必要があります。プロトンの数は現在電子の数を1つ超えているため、原子の正味の正電荷は+1であり、ルビジウム-85イオンになります。
電子を失うこのプロセスは、通常、化学反応または熱や光などの外部エネルギー源との相互作用の結果であり、電子と積極的に帯電した核との間の引力を克服するのに十分なエネルギーを提供します。