1。原子構造 :水素には1つのプロトン、1つの電子、および中性子はありません。それは、その核に単一の陽子を持つ唯一の要素です。球状の原子軌道で核の周りの電子軌道。
2。二等珪藻分子 :水素は通常、2つの水素原子が共有結合して結合している珪藻分子(H2)として存在します。 H-H結合は、最も強力な化学結合の1つであり、かなりの量のエネルギーを壊す必要があります。
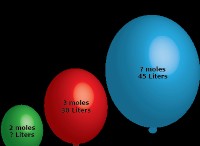
3。低密度 :水素の密度は非常に低く、最も軽い要素です。室温と圧力では、水素ガスの密度は1リットルあたり約0.09グラムです。
4。熱伝導率 :水素は、すべてのガスの熱伝導率が最も高い。これは、熱を非常に効率的に伝達できることを意味します。
5。可燃性 :水素は非常に可燃性であり、点火源の存在下で簡単に発火する可能性があります。それは淡い青い炎で燃え、大量の熱と水蒸気を放出します。
6。反応性 :水素は、他の元素と容易に化合物を形成する反応性要素です。酸素と反応して水を形成し、炭素と炭化水素を形成し、金属を形成して水素化物を形成することができます。
7。燃料 :水素は、車両の燃料電池や発電など、さまざまな用途向けの有望な燃料源と見なされます。単位の質量あたりのエネルギー含有量が高く、燃焼したときに副産物として水のみを生成します。
8。存在量 :水素は宇宙で最も豊富な要素であり、宇宙のすべての原子の約92%を占めています。主に星や巨大な惑星の分子水素型(H2)に見られます。
9。同位体 :水素には、3つの天然に存在する同位体があります。プロトウム(1つのプロトンを含む一般的な水素)、重水素(1つのプロトンと1つの中性子を含む重水素)、およびトリチウム(1つのプロトンと2つの中性子を含む放射性水素)。
10。アプリケーション :水素には、ロケットや燃料電池用の燃料、肥料の生産、石油の精製、プラスチックと化学物質の製造、および冶金など、さまざまな用途があります。
全体として、水素は、さまざまな科学、産業、技術の分野で重要になるユニークな特性を備えた用途の広く不可欠な要素です。