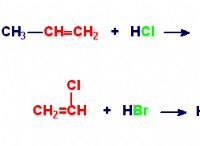
$$ cu(s) + h_2so_4(aq)→cuso_4(aq) + h_2(g)$$
この反応では、銅金属は硫酸と反応して硫酸銅と水素ガスを形成します。反応は次のように進行します:
1。銅金属原子はそれぞれ2つの電子を失い、銅イオン(Cu2+)を形成します。
2。硫酸中の水素イオン(H+)は、銅原子によって失われた電子と結合して水素ガス(H2)を形成します。
3.溶液中の銅イオンと硫酸イオン(SO42-)が結合して硫酸銅を形成します。
反応は発熱性であり、熱を放出することを意味します。反応の速度は、混合物を加熱するか、鉄(III)などの触媒を追加することで増加させることができます。