これが説明です:
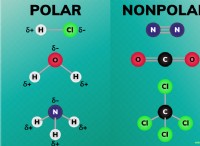
* 水分子は極性です: 水分子の酸素原子はわずかに負の電荷を持ち、水素原子にはわずかに正電荷があります。この極性により、水分子は互いに水素結合を形成できます。
* 液体水中の水素結合: 液体の水では、これらの結合が絶えず形成され、破壊されているため、分子は自由に移動し、比較的近くに梱包できます。
* 氷の水素結合: 水が凍結すると、水素結合はより安定し、固定の結晶構造に分子を保持します。この構造は、分子の間に大きな空間を備えた開いた六角形の格子によって特徴付けられます。
* 低密度: これらの大きなスペースのため、氷は液体水よりも密度が低くなっています。これが氷が浮かぶ理由です!
要約すると、水分子間の安定した水素結合に起因する氷の開放的な結晶構造は、液体水と比較して密度が低くなります。