これが彼らがそんなに反応的である理由です:
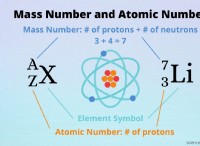
* 1つの価電子: アルカリの金属は、最も外側のシェル(価数シェル)に1つの電子しかありません。この単一の電子はゆるく保持され、簡単に失われ、正のイオン(+1電荷)を形成することを熱望しています。
* 低イオン化エネルギー: この単一の原子価電子を除去するのに非常に少ないエネルギーが必要であり、それらを非常に反応性にします。
* 大きな原子半径: それらの大きな原子半径は、外側の電子が核から遠く、密着していないことを意味します。
* 強力な電気陽性の性質: アルカリ金属は、電子を失い、陽性イオンを形成する強い傾向があるため、他の元素、特に非金属と容易に反応します。
アルカリ金属の例:
*リチウム(li)
*ナトリウム(NA)
*カリウム(K)
*ルビジウム(RB)
*セシウム(CS)
*フランシウム(FR)
反応性がグループを下回ります:
グループを下に移動すると、アルカリ金属の反応性が増加します。これは、原子半径が増加し、価電子を核からさらに遠ざけ、除去しやすくするためです。
安全ノート: アルカリ金属は水と空気で激しく反応するため、極度の注意を払って処理し、不活性雰囲気に保存する必要があります。