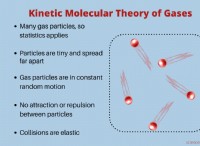
* 分子自由の増加: ガスは、液体や固体と比較して、移動の自由度がはるかに高くなります。彼らはより多くの翻訳、回転、振動の自由度を持っています。 より多くのガス分子を生成する反応、またはより制限された状態からガス分子が形成される場所は、一般にエントロピーの増加につながります。
* ボリューム拡張: より多くのモルのガス分子を生成する反応は、より大きな体積膨張につながります。この拡張により、システムの可能なマイクロステート(配置)の数が増加し、エントロピーが高くなります。
例:
* メタンの燃焼: CH4(g) + 2O2(g)→CO2(g) + 2H2O(g)
*製品のモルが少ないガスのモルが少ないが、水蒸気(高温では気体)の形成により、分子の自由と体積の膨張が増加するため、エントロピーの正味の増加につながります。
* 炭酸カルシウムの分解: Caco3(s)→Cao(s) + Co2(g)
*固体反応物からの気体CO2の形成は、システムのエントロピーを大幅に増加させます。
重要な考慮事項:
* 例外: いくつかの反応は、たとえそれがガスを含む場合でも、産物が反応物よりも順序付けられている場合、エントロピーが減少する可能性があります。たとえば、ガスの二量体化により、より大きな分子を形成します。
* 温度: エントロピーの変化も温度の影響を受けます。 より高い温度では、ガス分子はより大きな運動エネルギーを持ち、エントロピーを増加させます。
要約:
ガス反応のエントロピーの変化は、主に、より多くのガス分子が生成されるときに発生する分子の自由と体積の拡大の増加によって促進されます。例外が存在しますが、一般的な傾向はエントロピーの増加に向けています。