その理由は次のとおりです。
* イオン化エネルギー: 原子から電子を除去するために必要なエネルギーの量は、イオン化エネルギーと呼ばれます。
* 最も外側のシェルの電子: 最も外側のシェル(価電子)の電子は核から遠くにあり、核の正電荷からの魅力が少なくなります。これにより、削除が簡単になります。
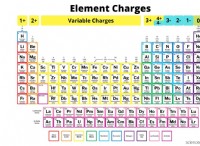
* 硫黄の電子構成: 硫黄には電子構成があります:1S²2S²2P⁶3S²3P⁴。 3P電子は最も外側であり、最も魅力的ではありません。
要約すると、硫黄の3Pサブシェルの電子は、核から最も遠く、最も弱い引力を経験するため、除去するために最小のエネルギーを必要とします。