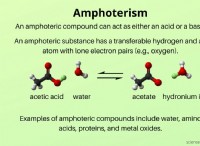
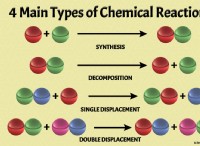
* 原子構造: 左から右に移動すると、核内の陽子の数が増加します。この正電荷の増加は、負に帯電した電子をより強く引き付け、電子雲を核に近づけます。
* ナトリウム対塩素:
* ナトリウム(Na): 11個のプロトンと11個の電子があります。その最も外側の電子は3S軌道にあります。
* 塩素(cl): 17個のプロトンと17個の電子があります。その最も外側の電子は、3Sおよび3p軌道にあります。
* サイズに対する効果: 塩素はより大きな核電荷(より多くの陽子)を持っているため、その電子はよりしっかりと描かれています。これにより、塩素が小さくなります 両方の元素が同じエネルギーレベル(3番目のエネルギーレベル)に最も外側の電子を持っているにもかかわらず、ナトリウムよりも。
要約:
* ナトリウム(Na): その核と最も外側の電子の間の魅力が弱いため、より大きな原子サイズ。
* 塩素(cl): その核と最も外側の電子の間のより強い引力による原子サイズが小さい。
他に質問がある場合はお知らせください!