1。物質に存在する要素: 物質を構成する要素のシンボルを示しています。たとえば、H₂Oは、水に水素(H)と酸素(O)が含まれていることを示しています。
2。各要素の原子の相対数: 各要素シンボルに従うサブスクリプトは、物質の1つの分子または式単位のその要素の原子の数を示しています。 H₂Oでは、添え字式「2」は、1つの酸素原子ごとに2つの水素原子があることを示しています。
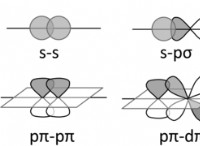
3。原子間の結合のタイプ: 式は、存在する結合の種類を示唆することがあります。たとえば、イオン化合物は通常、その経験的式(原子の最も単純な全自由比)で表されますが、共有化合物は分子の実際の原子数を示す分子式を使用します。
4。物質の分子量: 式のすべての原子の原子質量を合計することにより、化合物の分子量を計算できます。
5。物質の化学的特性: この式は、反応性や融点など、物質の特定の特性を予測するために使用できます。
ただし、化学式は常に発現するとは限りません:
* 空間内の原子の実際の配置: たとえば、フォーミュラc₂h₆は、異なる構造を持つエタンとプロパンの両方を表すことができます。
* 物質の物理状態: 式では、物質が特定の温度と圧力で固体、液体、またはガスであるかどうかはわかりません。
* 物質を生成した化学反応: フォーミュラは考えられる反応を示唆するかもしれませんが、その形成に伴う特定のステップはあなたに与えません。
したがって、化学式は物質の組成を要約するのに非常に役立ちますが、化合物のあらゆる側面を伝えません。