共有結合の基本
* 電子の共有: 共有結合では、原子は電子を共有して安定した電子構成を実現し、通常は貴重なガスに似ています。
* 最も外側のシェル: この共有は、主に価数シェルとも呼ばれる最も外側の電子シェルで発生します。
* 安定性: 電子を共有することにより、原子は原子価殻を完成させ、安定性を獲得します。
プロセス
1。オーバーラップ: 2つの原子が互いに近づくと、その原子価のシェルが重複し始めます。
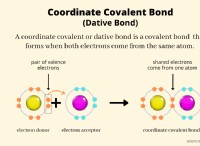
2。共有: 重複する領域の電子は、2つの原子間で共有されています。この共有電子のペアは、「結合ペア」と呼ばれます。
3。安定した構成: 現在、各原子には完全な価数シェルがあり、分子の安定性に寄与しています。
例:水(h₂o)
* 酸素(O): 6つの価電子(2S²2P⁴)があります。完全な外側のシェル(ネオンのような)を持つには、さらに2つの電子が必要です。
* 水素(H): 1つの価電子(1S¹)があります。完全な外側シェル(ヘリウムのような)を持つには、さらに1つの電子が必要です。
* 水の形成: 酸素原子は、各水素原子とその電子の1つを共有しています。 各水素原子は、その電子を酸素原子と共有しています。これにより、2つの共有電子ペアが発生し、2つの共有結合を形成し、各原子に安定した構成を与えます。
キーポイント
* 共有結合の種類:
* 単一の共有結合: 1つの共有電子のペア(例:h₂o)
* 二重共有結合: 電子の2つの共有ペア(たとえば、o₂)。
* トリプル共有結合: 3つの共有電子ペア(例:n₂)。
* 極性共有結合: 場合によっては、電子は均等に共有されません。電子に強い引っ張りを持つ原子はわずかに負になり、他の原子はわずかに正しくなります。これにより、水(H₂O)のような極性分子が作成されます。
本質的に、共有結合には原子の外殻内の電子の共有が含まれ、関連する両方の原子の安定した構成につながります。