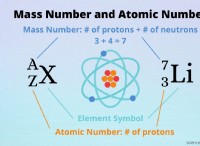
* 陽子: 核に見られると、陽子は正電荷を運びます。プロトンの数は要素を定義します。たとえば、すべての炭素原子には6つのプロトンがあり、すべての酸素原子には8つのプロトンなどがあります。この数字はアトミック番号と呼ばれます。
* 中性子: また、核に位置する中性子には電荷がありません。中性子の数は要素内で異なる場合があり、同位体が生成されます。同じ元素の同位体は、同じ数のプロトンを持っていますが、中性子の数は異なります。たとえば、炭素12には6つの中性子があり、炭素-14には8つの中性子があります。
* 電子: 核を軌道に乗せていることがわかり、電子は負電荷を運びます。 原子は一般にプロトンと同じ数の電子を持ち、電気的に中性にします。
これが重要な違いを要約するテーブルです。
|機能|陽子|中性子|電子|
| --- | --- | --- | --- |
| 電荷 |ポジティブ(+)|ニュートラル|負( - )|
| 場所 |核|核|軌跡核|
| を決定します |要素|同位体|化学的挙動|
要約:
* 要素 プロトンの数(原子数)によって定義されます。
* 同位体 同じ要素の数は同じ数のプロトンですが、中性子の数は異なります。
*電子の数 一般に、プロトンの数と一致しますが、正味の電荷があるイオンでは異なる場合があります。
陽子、中性子、および電子の数の違いは、原子の原子質量、その化学的性質、およびその全体的な安定性を決定します。これらの違いは、宇宙のすべての物質の多様性と行動を理解するために重要です。