その理由は次のとおりです。
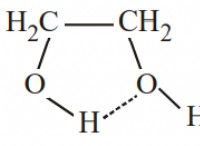
* "like like dislols like": 化学の一般的な経験則は、同様の極性のある物質が互いに溶解する傾向があるということです。水は極性分子であり、つまり、わずかに正の端とわずかに負の端を持っています。
* 極性溶質: 水は、塩(塩化ナトリウム)、糖(グルコースなど)、および多くの酸と塩基などの極性物質を容易に溶解します。水分子の極端は、これらの溶質の極端な端と強いアトラクション(水素結合)を形成し、それらを引き離して溶解することができます。
* 非極性溶質: 水は、油、脂肪、多くの有機化合物などの非極性物質を溶解しません。これらの物質には、強力な魅力を形成するために水分子が必要とする帯電した領域がありません。
例:
* 塩は水に溶けます: 塩はイオン性であり、荷電粒子(イオン)を形成することを意味します。水分子はこれらのイオンを囲み、それらを引き離します。
* オイルは水に溶けません: オイルは非極性であり、水分子と強く相互作用しません。
したがって、物質を溶解する水の能力は、水分子と溶質分子間の相互作用の極性と相互作用の強さに依存します。