* 原子には質量が異なります: 各要素には異なる原子質量があります。たとえば、炭素原子は金の原子よりもはるかに軽いです。
* 質量は物質の量の尺度です: 68.0 kgは特定の量の問題を表していますが、どのような問題を教えてくれません。
原子の数を計算するには、が必要です
1。物質の化学式: これは、どの要素が存在するか、どの比率にあるかを示します。
2。 Avogadroの番号: この定数は、モル(6.022 x 10^23原子/mol)の原子数を関連付けます。
これがそれを行う方法です:
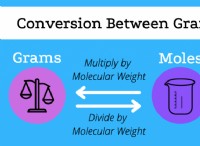
1。モル数を計算します: 質量(68.0 kg)を物質のモル質量で除算します。
2。 Avogadroの番号:を掛けます これにより、その多くのほくろの原子の数が得られます。
例:
68.0 kgの純金(AU)で原子の数を見つけたいとしましょう。
1。金のモル質量(au): 196.97 g/mol
2。 kgをg:に変換します 68.0 kg * 1000 g/kg =68000 g
3。モルを計算: 68000 g / 196.97 g / mol =345.2 mol
4。原子の計算: 345.2 mol * 6.022 x 10^23 Atoms/mol = 2.08 x 10^26 Atoms
要約すると、特定の質量の原子数を決定するために特定の物質を知る必要があります。