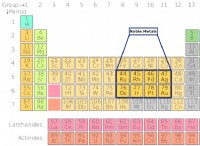
その理由は次のとおりです。
* 中性原子: 酸素原子には8つのプロトン(正電荷)と8つの電子(負電荷)があります。これらの電荷はバランスを取り、原子を電気的にニュートラルにします。
* 酸化状態: 酸素は非常に感動的であるため、電子を強く引き付けることを意味します。化合物では、しばしば電子を獲得し、負の酸化状態を形成します 、通常-2。これは、永続的な電荷を持っているという意味ではなく、むしろ化合物の相対電子分布を示しています。
例:
* 水(h₂o): 酸素は電子を2つの水素原子と共有し、-2酸化状態を与えます。
* 二酸化炭素(CO₂): 酸素は電子を炭素と共有し、再び-2酸化状態を持っています。
イオン: 酸素は、酸化物(o²⁻)と呼ばれるイオンを形成できます 2つの電子を獲得することにより。このイオンには-2電荷があります。
要約:
* 酸素原子: 中性。
* 化合物中の酸素: 多くの場合、-2酸化状態があります。
* 酸化物イオン: -2充電。