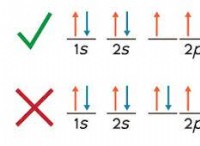
* 塩素の電子構成: 塩素には17個の電子があります。その電子構成は2-8-7です。つまり、最も外側のシェル(3番目のシェル)に7つの電子があります。
* オクテットルール: 原子は、最も外側のシェルに8つの電子がある場合に最も安定している傾向があります(水素とヘリウムを除き、2つだけが必要です)。これはOctetルールとして知られています。
* 安定性に対する塩素の必要性: 塩素には外殻に7つの電子があるため、安定したオクテットを達成するにはもう1つの電子が必要です。
塩素が安定性をどのように達成するか:
安定するために、塩素は次のとおりです。
* 電子を獲得: これは、負電荷を持つ塩化物イオン(CL-)を形成します。これは、塩素がイオン化合物の安定性を達成する一般的な方法です。
* 電子を共有: 塩素は、電子を共有することにより、他の原子と共有結合を形成できます。これは、塩素が塩素ガス(CL2)のような分子を形成する方法です。
要するに 塩素は安定するために1つの電子を獲得する必要があります。これは、イオン結合または共有結合を形成することでこれを達成できます。