1。それは最小の原子です: これは、その単一のプロトンと電子が非常に近くにあることを意味し、核に高い濃度の正電荷をもたらすことを意味します。
2。共有結合とイオン結合の両方を形成できます: 水素の電子を共有または失う能力は、多用途になります。
* 共有結合: これらの結合では、水素は、水(H₂O)やメタン(Ch₄)などの別の原子とその電子を共有しています。
* イオン結合: 水素はまた、その電子を失い、正の帯電イオン(H+)を形成し、塩酸(HCl)のようにイオン結合を作り出します。
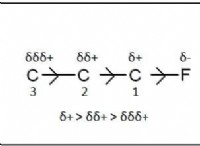
3。水素結合: 水素のユニークな特性は、水素結合と呼ばれる特別なタイプの分子間力を生じさせます 。これは、水素原子が酸素、窒素、またはフッ素のような高強性原子に共有結合したときに発生します。水素原子は部分的に陽性になり、隣接する電気陰性原子に孤立した電子のペアを引き付けます。
* 最も強い分子間力: 水素結合は、分子間力の最も強いタイプであり、次のような特性にとって重要になります。
* 高沸点: たとえば、水は水素結合により高い沸点を持っています。
* 溶解度: 水素結合相互作用のために、多くの物質が水に溶けます。
* DNA構造: 水素結合は、DNAの2つの鎖を一緒に保持します。
4。多くの反応に参加する能力: 水素の反応性とサイズが小さいため、以下を含む多くの化学反応の重要なプレーヤーになります。
* 燃焼: 水素は酸素で容易に燃焼して水を生成し、エネルギーを放出します。
* 酸塩基反応: 水素イオン(H+)は、酸塩基反応において中心的な役割を果たします。
要約すると、水素の特別な特性は、その小さなサイズ、異なる結合タイプを形成する能力、および水素結合に参加するユニークな能力から生じます。これにより、化学と生物学の多くの分野で水素が不可欠な要素になります。