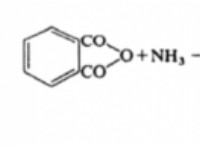
1。化学式:
* 反応を表す最も基本的で基本的な方法。 シンボルを使用して、反応物(出発材料)と生成物(結果として生成される物質)を示し、化学量論係数(それぞれの相対量を示す)を示します。
* 例: 2H₂ +o₂→2H₂O(この方程式は、2つの水素ガスの分子が酸素ガスの1つの分子と反応して2つの水分を生成することを示しています。)
* 制限: それは全体的な変化のみを示しており、ステップバイステップのプロセスや関連するエネルギーではありません。
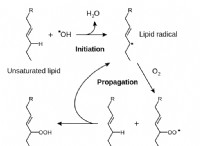
2。反応メカニズム:
* 反応中に発生する個々のステップのシーケンスを説明します。 これには、中間体の形成、結合の破壊と形成、および各ステップの活性化エネルギーが含まれます。
* 例: メタン(Ch₄)の燃焼には、フリーラジカルの形成やエネルギーの放出など、いくつかのステップが含まれます。
* 利点: 反応がどのように進行するかをより深く理解します。
3。熱力学:
* 反応中のエネルギーの変化に焦点を当てています。 エンタルピー(熱変化)、エントロピー(障害)、ギブスの自由エネルギーなどの概念を使用して、反応の実現可能性と自発性を予測します。
* 例: 水素と酸素と水を形成することの反応は発熱性であり、熱としてエネルギーを放出します。
* 利点: 特定の条件下で反応が発生するかどうか、および放出または吸収されるエネルギーの量を予測するのに役立ちます。
4。速度論:
* 反応の速度を研究しています。 温度、濃度、触媒など、反応速度に影響を与える要因を調べます。
* 例: 反応の温度を上げると、通常、分子の運動エネルギーが高いため、反応速度が増加します。
* 利点: 効率と制御のための反応条件を最適化するのに役立ちます。
5。分光分析:
* さまざまな手法を使用して反応物と産物を分析し、それらの構造と特性に関する情報を提供します。 一般的な手法には、赤外線(IR)分光法、核磁気共鳴(NMR)分光法、および質量分析が含まれます。
* 例: IR分光法は、分子内の特定の官能基を特定し、反応中に発生した化学変化を理解するのに役立ちます。
* 利点: 反応中に発生する分子変換に関する詳細な洞察を提供します。
6。視覚化とアニメーション:
* 3Dモデルとアニメーションを使用して、原子レベルと分子レベルでの反応プロセスを表す これらは、原子の動き、結合の破壊と形成、および関連するエネルギーの変化を視覚化するのに役立ちます。
* 利点: より直感的で魅力的な反応を提供します。
最終的に、化学反応の「ストーリー」は、これらの異なるソースからの情報を組み合わせることによって語られます。収集する情報が多いほど、より完全で微妙な理解になります。