これが故障です:
* 反応性: 元素が化学反応を受ける程度の尺度。
* 容易さ: 化学反応に参加する要素の傾向を指します。一部の要素は容易に反応しますが、他の要素は反応性が低くなります。
* 速度: 化学反応が発生する速度を指します。高度な反応性要素は迅速に反応する傾向がありますが、反応性要素が少ない場合はゆっくりと反応するか、まったく反応しない場合があります。
反応性に影響する要因:
* 電子構成: 元素の原子内の電子の配置は、化学反応を促進する電子を獲得、失い、または共有する傾向を決定します。
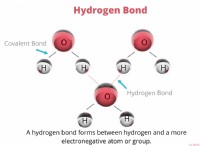
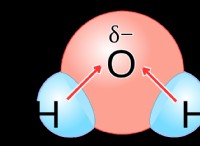
* 電気陰性度: 化学結合に電子を引き付ける原子の能力。より多くの電解要素はより反応的になる傾向があります。
* イオン化エネルギー: 原子から電子を除去するために必要なエネルギー。イオン化エネルギーが低い元素は、電子を失い、反応する可能性が高くなります。
* 原子サイズ: より大きな原子は一般に、最も外側の電子に対するより弱いアトラクションを持ち、それらをより反応的にします。
例:
* ナトリウム(Na) 最も外側の電子を容易に失い、正のイオンを形成するため、非常に反応性があります。
* 金(au) 電子がしっかりと保持されており、それらを除去することが困難であるため、非常に非アクティブです。
反応性を理解することは、さまざまな化学環境で要素がどのように動作するかを予測するのに役立つため、化学において重要です。