1。電子構成:
*硫黄の原子数は16です。つまり、16個の電子があります。
*その電子構成は次のとおりです:1S²2S²2P⁶3S²3P⁴
2。 軌道図:
* 3Pサブシェルには3つの軌道(3px、3py、3pz)があります。
*各軌道は、反対のスピンを持つ最大2つの電子を保持できます。
* Hundのルールに従って、軌道を3pサブシェルの4つの電子で満たします(各軌道はペアになる前に1つの電子を取得します)。
これが軌道図です:
`` `
3px 3py 3pz
↑↑↓
`` `
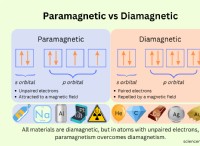
3。対応のない電子:
*ご覧のとおり、 2つのがあります 硫黄の無気力な電子。