これがバランスの取れた化学式です:
h₂c₂o₄(aq) + 2nh₄oh(aq)→(nh₄)₂c₂o₄(aq) + 2h₂o(l)
説明:
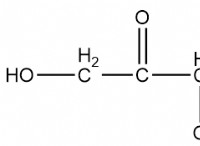
* シュウ酸 双トロス酸です。つまり、2つの水素イオン(H⁺)を寄付できることを意味します。
* 水酸化アンモニウム 弱い塩基で、水酸化物イオン(OH⁻)を提供します。
*これらが反応すると、酸からのh⁺は、基部からのOh⁻と結合して水を形成します。
*残りのイオン、アンモニウム(nh₄⁺)およびシュウ酸塩(c₂o₄²⁻)は、塩シュウ酸アンモニウムを形成します 。
観測:
*反応は発熱性であり、熱を放出します。
*反応物の濃度が高い場合、シュウ酸アンモニウムの白い沈殿物が形成される可能性があります。
使用:
*シュウ酸アンモニウムは、カルシウムおよび他の金属の沈殿剤として分析化学で使用されます。
*染色の媒染剤として、および写真の還元剤としても使用されます。