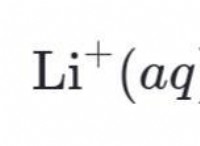* 吸熱反応: これらの反応は、周囲から熱を吸収します。これは、反応物の結合を破るためにエネルギーが必要であり、製品に新しい結合が形成されると、より少ないエネルギーが放出されることを意味します。
* 塩化アンモニウムの溶解: 塩化アンモニウムが溶解すると、次のことが起こります。
* 破壊債: 結晶格子内のアンモニウム(NH₄⁺)と塩化物(Cl⁻)イオンを保持するイオン結合は壊れなければなりません。これには、周囲から吸収されるエネルギーが必要です。
* 水分補給: 水分子はイオンを囲み、水和シェルを形成します。このプロセスはある程度のエネルギーを放出しますが、イオン結合を破るために必要なエネルギーよりも少ないです。
* ネットエネルギーの変化: 水分補給中に放出されるよりも多くのエネルギーが結合を破るために吸収されるため、全体的なプロセスは吸気性です。これは、ソリューションが周囲から熱を吸収し、ビーカーを冷たく感じさせることを意味します。
簡単に言えば:
このようなプロセスを考えてみてください。あなたは、しっかりと詰め込まれた人々のグループ(塩化アンモニウム結晶)を分解しようとしています。それらを分離するには努力(エネルギー)が必要です。 次に、友人のグループ(水分子)で一人一人を囲みます。これにより、ある程度のエネルギーが解放されますが、最初の努力を補うには十分ではありません。 周囲(ビーカーとあなたの手)からエネルギーが奪われたので、彼らは冷たく感じます。