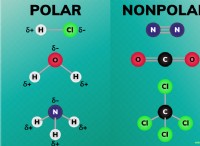
定比例の法則 単一の化合物のサンプルには、質量で同じ割合の元素が含まれていると述べています。法則の別名はプルーストの法則 または定数合成の法則 .どちらの名前を使用しても、この法則と複数の比率の法則が化学の化学量論の基礎を形成します。
定比例の法則の例
たとえば、水素と酸素の質量比は、純水 (H2 O)。水のモル質量は、酸素原子の質量に追加された水素原子の質量です。これらの数字は周期表にあります。
水の質量 =(2 x 水素の質量) + 酸素の質量 =(2 x 1.01) + 16.00 =18.02
水素は化合物の質量の 11.19% を占めます:
% 水素 =2.02/18.02 =0.112 =11.2%
% 酸素 =16.00/18.02 =0.888 =88.8%
別の見方をすれば、水は常に質量で 1/9 の水素と 8/9 の酸素であるということです。
定義比率の法則は、イオン化合物にも適用されます。たとえば、食卓塩または塩化ナトリウムの式は NaCl です。ナトリウムの原子質量は約 23 で、塩素の質量は約 35 です。元素間の質量比に基づいて、58 グラムの NaCl を解離すると、23 グラムのナトリウムと 35 グラムの塩素が生成されると予想されます。
同じ元素からなる 2 つの化合物の質量比が互いに異なる場合、それらは 2 つの異なる化合物であることがわかります。したがって、CO と CO2 など、同じ元素を使用する 2 つの式を持つサンプルがある場合 、あなたはそれらが完全に異なる化合物であることを知っています.
定比例の法則の例外
定比例の法則には例外があります。非化学量論的化合物は、サンプルごとに質量組成が異なります。たとえば、ウスタイトと呼ばれる酸化鉄鉱物の化学式は Fe0.95 です。 結晶構造が化学量論比からのわずかなずれを許容するため、FeO ではなく O です。
同位体は、化合物の質量組成にも影響を与えます。特定の元素の同位体の比率は、そのソースによって異なります。これは、異なる要素の質量比を持つ異なる場所からのサンプルにつながります。通常、化合物に水素が含まれていない限り、質量差は小さいです。
ポリマーは、含まれるモノマーの数に応じて、質量による元素組成も異なります。ただし、それらの化学式は通常、一定の比率の法則に従う化学量論比です。
歴史
この法則を発見した功績は、1797 年にそれを記述したフランスの化学者ジョセフ・プルーストの功績によるものです。ジョセフ・プリーストリーとアントワーヌ・ラヴォアジエも、元素が一定の割合で結合する方法を観察しました。
定義比率の法則は、日常の化学計算において重要ですが、歴史的な意味もあります。これは、ジョン・ダルトンの 1803 年の原子論を支持する法則の 1 つです。
参考文献
- ジョージ・ガモウ (1987)。 One Two Three… Infinity:Facts and Speculations of Science (バンタム科学と数学編)。バンタム。 ISBN 978-0486256641。
- Geng, Hua Y.;ら。 (2012)。 「点欠陥の疑似相転移によって引き起こされる非化学量論的二酸化ウランの異常」。 Phys. Rev. B . 85 (14):144111. doi:10.1103/PhysRevB.85.144111
- Greenwood, N.N.;アーンショー、A. (2012)。 元素の化学 (第 2 版)。エルゼビア。 ISBN 0080501095.
- プルースト、J.-L. (1806)。 「Sur les mines de Cobalt, Nickel et autres」. Journal de Physique . 63:566-8.
- Zumdahl, S. S. (1986) 化学 .マサチューセッツ州レキシントン。 ISBN 0-669-04529-2.