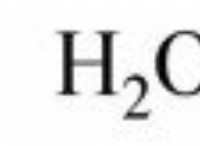1。イオン水素化物:
これらは、主にグループ1と2(アルカリとアルカリの土砂)から、次のような最も電気依存症の金属で形成されます。
* リチウム(li)
* ナトリウム(Na)
* カリウム(k)
* ルビジウム(RB)
* cesium(cs)
* ベリリウム(be)
* マグネシウム(mg)
* カルシウム(Ca)
* strontium(sr)
* バリウム(BA)
イオン水素化物では、水素原子が電子を獲得して水素化物イオン(H-)を形成し、金属陽イオンとイオン結合を形成します。これらの化合物は通常、室温で結晶固体であり、非常に反応性があります。
2。共有水素化物:
これらは、次のような遷移金属で形成されます。
* チタン(TI)
* ジルコニウム(Zr)
* Hafnium(HF)
* バナジウム(v)
* ニオビウム(NB)
* Tantalum(Ta)
* クロム(Cr)
* モリブデン(MO)
* タングステン(w)
共有水素化物では、水素原子は電子を金属原子と共有し、共有結合を形成します。これらの化合物は、室温の固体、液体、またはガスであり、イオン水素化物よりも幅広い特性を示します。
注:
*すべての金属が水素化物を形成するわけではありません。
*金属水素化物の形成と特性は、金属と水素の電気陰性度の違い、金属原子のサイズ、金属原子の空の軌道の可用性などの因子に依存します。
金属水素化物の応用:
金属水素化物には、以下を含むさまざまな用途があります。
* 水素貯蔵: 一部の金属水素化物は、大量の水素ガスを吸収および放出することができ、水素燃料の保管と輸送に役立ちます。
* バッテリー: 特定の金属水素化物は、ニッケルメタル水素化物などの充電式電池で使用されます。
* 触媒: 金属水素化物は、さまざまな化学反応の触媒として作用できます。
金属水素化物の研究は、さまざまな用途向けの特性が改善された新しい材料を開発するための継続的な取り組みを伴う、活発な研究分野です。