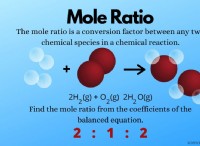
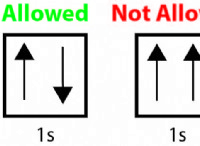
* pHスケール: pHスケールは、溶液の酸性度またはアルカリ度を測定します。範囲は0〜14です。
* 中和: 酸とベースが反応すると、それらはお互いを中和します。ニュートラルソリューションのpHは7です。
* pH未満82397: この値は非常に高く、pHスケールのコンテキストでは意味がありません。
これが意図されている可能性のあるものです:
この質問は、おそらく酸と塩基の組み合わせが常に7未満のpH の溶液をもたらすかを知りたいと思うことを望んでいます (溶液が酸性であることを意味します)。
説明:
* 強酸と強いベース: 強酸(例えば、塩酸、HCl)が強い塩基(例えば、水酸化ナトリウム、NaOH)と反応すると、結果の溶液は中性(pH 7)になります。
* 強酸と弱い塩基: 強酸が弱い塩基(例:アンモニア、NH3)と反応すると、得られる溶液はわずかに酸性になります(pH未満)。これは、弱い塩基が強酸を完全に中和しないためです。
* 弱酸と強いベース: 弱酸(酢酸、CH3COOHなど)が強い塩基と反応すると、結果の溶液はわずかに塩基性になります(pHが7を超えます)。
* 弱酸と弱い塩基: ここでの結果は予測が少なく、特定の酸と塩基に依存します。ただし、通常、わずかに酸性、わずかに塩基性、またはニュートラルに近いです。
したがって、強酸と弱い塩基の組み合わせは、常に7未満のpHの混合物を生成します。