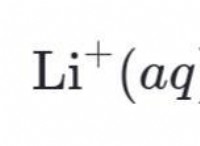cl₂(g) + 2 ki(aq)→2 kcl(aq) +i₂(s)
これが反応で起こることです:
* 塩素(Cl₂)は強力な酸化剤です: 電子を獲得し、負に帯電したいと考えています。
* ヨウ化カリウム(KI)のヨウ化イオン(I-)は簡単に酸化されます: 彼らはすぐに電子を失います。
反応で:
*塩素(Cl₂)は、ヨウ化カリウム(KI)からヨウ素(I₂)を変位させます。
*塩素(Cl₂)は電子を摂取し、塩化物イオン(Cl-)を形成し、カリウムイオン(K+)と結合して塩化カリウム(KCl)を形成します。
*ヨウ素(i₂)は酸化され、固体ヨウ素(i₂)を形成します。
この反応は、単一変位反応の典型的な例です より反応性の高いハロゲン(塩素)が、その化合物からあまり活性のないハロゲン(ヨウ素)を変位させる場合。