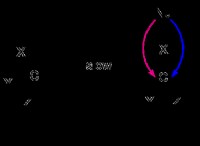
共有結合を座標
* 1つの原子が両方の電子を結合内の共有ペアに寄与すると、座標共有結合(dative結合とも呼ばれます)が発生します。
*電子ペアは、1つの原子の唯一のペアから他の原子の空の軌道に寄付されます。
分子の分析:
* HCl(塩化水素): これは通常の共有結合であり、各原子が1つの電子に寄与します。
* HF(フッ化水素): これは通常の共有結合でもあります。
* h₂o(水): 水には、酸素と水素原子の間に正常な共有結合が含まれています。 ただし、水中の酸素原子には2つの唯一の電子があることを理解することが重要です。これにより、水は座標共有結合を形成する際に良好な電子ドナーになります。
* h₃o⁺(ハイドロニウムイオン): これは、座標共有結合を見つける場所です!
* 層: h₃o⁺は、水分子(h₂o)が酸からプロトン(h⁺)を受け入れると形成されます。
* 結合: プロトン(H⁺)には空の軌道があります。水中の酸素原子の唯一のペアの1つは、この空の軌道との座標共有結合を形成します。
結論:
* h₃o⁺(ハイドロニウムイオン)には、座標共有結合が含まれています。
これらの分子のいずれかについてもっと説明したい場合はお知らせください!