1。バランスの取れた化学式を書きます:
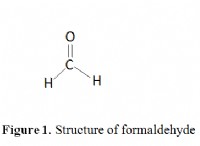
プロパナル(c₃H₆O)の燃焼は、二酸化炭素(CO₂)と水(H₂O)を生成します。
c₃h₆o +4o₂→3co₂ +3h₂o
2。水とプロパンのモル比を決定します:
バランスの取れた方程式から、1分のプロパナル(C₃H₆O)が3分の水(H₂O)を生成することがわかります。
3。水のモルをグラムに変換:
*水の臼歯質量(H₂O)は18.015 g/molです。
*モル比と水のモル質量を使用します。
3 molh₂o×18.015 g/mol =54.045 gh₂o
したがって、プロパナールの火傷1分の54.045グラムが形成されます。