基本を理解する
* 電気分解: 電気を使用して化合物をその要素に分解するプロセス。
* アノード: 電解セル内の正の電極。
* カソード: 電解セル内の負の電極。
化学
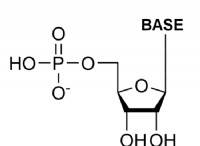
1。水の化学構造: 水(H₂O)は、水素原子にわずかに正電荷と酸素原子にわずかに負の電荷を伴う極性分子です。
2。電極引力:
* アノード(ポジティブ): 水酸化物イオン(OH⁻)のような負に帯電したイオン(アニオン)を引き付けます。
* カソード(負): 水素イオン(H⁺)のような積極的に帯電したイオン(陽イオン)を引き付けます。
3。アノードでの反応:
* 酸化: 電子を失うプロセス。アノードでは、水酸化物イオン(OH⁻)が電子を失い、酸素ガス(O₂)を形成します。
4OH⁻→2H₂O +o₂ +4e⁻
なぜ酸素が陽極で形成されるのか:
* 酸化: アノードの正電荷は、電子の損失を促進します(酸化)。水素よりも電気陰性である酸素は、酸素ガスを形成するために電子を容易に受け入れます。
* 水素イオン形成: 酸素ガスの形成は、カソードに向かって移動する水素イオン(H⁺)も生成します。
要約
アノードの正電荷と水酸化物イオンがこの電極で電子を失う傾向は、水の電気分解中に酸素ガスの形成につながります。