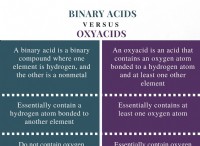
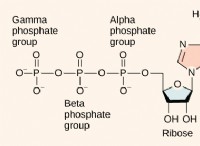
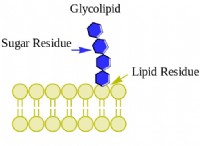
1。要素:
* 金属: ほとんどの金属は電子を失い、陽イオンになりがちです。
* 非金属: 一部の非金属もカチオンを形成することができますが、これはあまり一般的ではありません。
2。分子:
* 多原子イオン: これらは、正味の正電荷を運ぶ原子の結合グループです。例は次のとおりです。
*アンモニウムイオン(nh₄⁺)
*ハイドロニウムイオン(H₃O⁺)
重要な注意:
*陽イオンの電荷は、失われた電子の数によって決定されます。
*たとえば、ナトリウム原子(Na)は1つの電子を失い、ナトリウム陽イオン(Na⁺)になり、マグネシウム原子(mg)は2つの電子を失い、マグネシウム陽イオン(mg²⁺)になります。
カチオンの例:
* ナトリウムイオン(Na⁺)
* カルシウムイオン(ca²⁺)
* 鉄(ii)イオン(fe²⁺)
* アルミニウムイオン(al³⁺)
* 銅(i)イオン(cu⁺)
* アンモニウムイオン(nh₄⁺)
* ヒドロニウムイオン(H₃O⁺)
陽イオンはイオン化合物の必須成分であり、そこでは負に帯電した陰イオンを持つ静電結合を形成します(負電荷を持つイオン)。