1。バランスの取れた化学式を書きます:
Fe + S→FES
2。グラムをモルに変換します:
* Fe:
* fe =(25.0 g fe) /(55.845 g / mol fe)=0.447 mol feのモル
* s:
* s =(32.0 g s) /(32.065 g / mol s)=0.998 mol sのモル
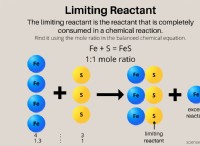
3。制限反応物を決定します:
*制限反応物は、最初に完全に消費されるものであり、形成された製品の最大量を決定します。
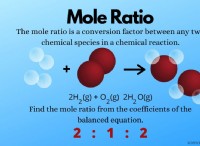
*バランスの取れた方程式から、feとsのモル比は1:1です。
* S(0.998 mol)よりもFe(0.447 mol)のモルが少ないため、Feは制限反応物です。
4。 FES:の理論的収量を計算します
* FEとFESのモル比も1:1です。
*したがって、FESの理論的収量は、Fe:0.447 mol FESのモルに等しくなります。
5。モルをグラムに変換します:
*グラム中のFESの理論収量=(0.447 mol FES) *(87.91 g/mol FES)= 39.3 g FES
したがって、 25.0 g Feおよび32.0 g sの反応が39.3 g Fes。の場合、FESの理論的収量は