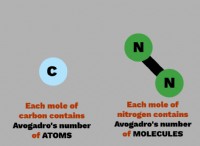
化合物
* 定義: 2つ以上の異なる元素が化学的に固定比で組み合わされたときに形成される純粋な物質。
* 層: 化合物内の元素は化学反応を起こし、元の要素とはまったく異なる特性を持つ新しい物質をもたらします。
* 構成: 化合物内の元素の比率は常に固定されています。たとえば、水(H₂O)には、すべての酸素原子に常に2つの水素原子があります。
* 分離: 化合物は、化学的平均(電気分解など)によってのみ、構成要素に分離できます。
* 例: 水(H₂O)、テーブルソルト(NaCl)、二酸化炭素(CO₂)
ソリューション
* 定義: ある物質(溶質)が別の物質(溶媒)に均等に溶解すると形成された均質な混合物が形成されます。
* 層: 溶質と溶媒は物理的に結合しますが、新しい化学結合は形成されません。
* 構成: 溶質と溶媒の比率は異なります。
* 分離: 溶液は、蒸発やろ過などの物理的手段によって分離できます。
* 例: 塩水(塩を水に溶解)、茶に溶解した砂糖、空気(空気に溶解したガス)。
重要な違い
|機能|化合物|解決策|
| --- | --- | --- |
| 形成 |化学反応、新しい物質が形成されました|物理的な混合、新しい物質は形成されませんでした|
| 構成 |要素の固定比|溶質と溶媒の可変比|
| 分離 |必要な化学的方法|可能な物理的方法|
| プロパティ |新しいプロパティが出現します|一般的に保持される元のプロパティ|
このように考えてみてください:
* 化合物: ケーキを焼くことを想像してみてください。小麦粉、砂糖、卵、バターを混ぜます。彼らは化学的に反応し、異なる味、テクスチャー、外観で新しい物質 - ケーキ - を作成します。
* 解決策: アイスティーを作ることを考えてください。砂糖を水に溶かします。砂糖は消えますが、水はまだ甘いです。水を沸騰させることで、砂糖と水を簡単に分離できます。
他に質問がある場合はお知らせください!