より詳細な説明を次に示します。
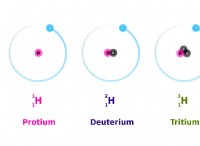
* 原子 物質の基本的な構成要素です。それらは、電子の雲に囲まれた陽子と中性子を含む核で構成されています。
* 分子 2つ以上の原子が結合すると形成されます。この結合は、原子が通常、最も外側の電子シェルを充填することにより、安定した電子構成を実現しようとしているために発生します。
* 共有結合 原子間の電子の共有を伴います。これらの結合は強力であり、通常、非金属原子間で形成されます。
* イオン結合 ある原子から別の原子への電子の伝達を伴い、イオン(正味の電荷を持つ原子)の形成をもたらします。このタイプの結合は、通常、金属と非金属の間に形成されます。
* 金属結合 多数の金属原子間で電子の共有を含みます。これは、金属の良好な導電率を可能にする「電子の海」の形成につながります。
分子の例:
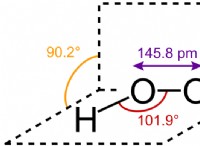
* 水(h₂o) - 酸素原子に共有結合した2つの水素原子。
* 二酸化炭素(CO₂) - 1つの炭素原子が2つの酸素原子に共有結合しました。
* 塩化ナトリウム(NaCl) -1つのナトリウムイオン(Na+)および1つの塩化物イオン(Cl-)は、イオン結合によって結合されています。
分子に関する重要なポイント:
*分子は、同じタイプの原子(酸素ガス、o₂など)または異なるタイプの原子(水、H₂Oなど)で構成できます。
*分子の特性は、多くの場合、それを構成する個々の原子の特性とは異なります。
*分子は絶えず動いており、互いに相互作用しているため、さまざまな物理的状態(固体、液体、ガス)があります。
分子を理解することは、私たちの周りの世界で起こる物質の性質と化学反応を理解するための基本です。