その理由は次のとおりです。
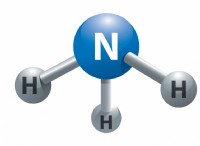
* 極性: 水分子は曲がった形状で、酸素はわずかに負に帯電し、水素がわずかに正に帯電しています。この不均一な電荷分布は双極子モーメントを作成し、水を極地にします。
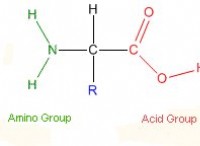
* アトラクション: 水分子の正の端は、他の極性分子(糖、塩、アルコールなど)の負の端に引き付けられ、その逆も同様です。この魅力は、溶質分子を分解し、水に溶けるのに役立ちます。
* 水素結合: 水分子は、互いに、および他の極性分子と水素結合を形成できます。これらの結合は強力であり、溶解した物質を溶液中に保つのに役立ちます。
対照的に、非極性分子(油や脂肪など)は、水分子と相互作用する極性の性質がないため、水に容易に溶解しません。