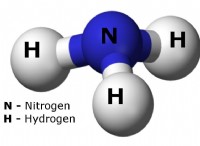
* 分子形状: NCL₃は三角錐体形状です。窒素原子は中心にあり、3つの塩素原子が付いており、窒素上に孤立した電子のペアが付いています。
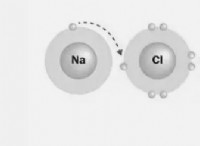
* 電気陰性の差: 塩素は窒素よりも電気陰です。これは、塩素原子がN-cl結合の共有電子をそれ自体に近づけ、塩素原子に部分的な負電荷(Δ-)を作成し、窒素原子に部分的な正電荷(Δ+)を作成することを意味します。
* 非対称電荷分布: 窒素原子の3つの極性N-CL結合と孤立したペアは、互いにキャンセルしません。これにより、分子に正味の双極子モーメントが作成され、塩素原子に向けられます。
したがって、極性N-CL結合と非対称電荷分布のため、ncl₃は極性分子です。