* 「分子に原子を一緒に保持する力」 分子内の力を参照してください 、共有結合やイオン結合のように。
* 「ガスを一緒に保持する力」 分子間力を参照してください 、ファンデルワールスの力や水素結合のように。
分子内の力が分子間力よりも強い理由は次のとおりです。
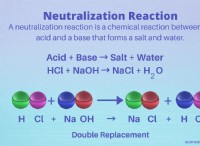
* 分子内の力には、電子の共有または伝達が含まれます 原子間で、安定した分子に原子を一緒に保持する強力な静電引力を作成します。
* 分子間力はより弱い魅力です これは、電子分布の一時的な変動または永久双極子のために分子間で発生します。これらの力は、分子内で原子を一緒に保持する力よりもはるかに弱いです。
ここに簡単なアナロジーがあります:
手を握っている2人がいると想像してください(分子内の原子を表しています)。この手持ちは強く、壊れるのが困難です(分子内絆を表しています)。ここで、ロープのネットワーク(分子間の力を表す)によって大まかに接続されている人々の大規模なグループがあると想像してください。これらのロープは、手持ちよりもはるかに弱く、壊れやすいです。
要約:
分子(分子内の力)に原子を一緒に保持する力は、前者は電子の共有または伝達により原子間のより強い静電誘引を伴い、後者は分子間のより弱い魅力であるため、分子(分子間力)に分子を保持する力よりも強いです。