これが故障です:
* イオン化合物: これらの化合物は、正に帯電した陽イオンと、強い静電力によって結合された負に帯電した陰イオンで構成されています。
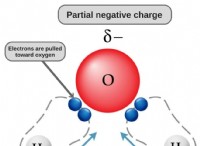
* 溶媒: 溶媒は、他の物質を溶解できる物質です。水のような極性溶媒は、電子の不平等な共有のために正と負の末端(双極子)を持つ分子を持っています。
* 溶解プロセス: 水のような極性溶媒がイオン化合物に遭遇すると、水分子の正の端がイオン化合物の陰イオン(陰イオン)を引き付け、水分子の負の端は陽イオン(陽イオン)を引き付けます。 この魅力は、イオンを固体で一緒に保持する静電力を弱めます。
* 水分補給(または溶媒和): その後、水分子は個々のイオンを囲み、水分補給の球体を形成します。溶媒和と呼ばれるこのプロセスは、イオンを互いに効果的に分離し、イオン格子の再形成を防ぎます。 その結果、イオン化合物が溶解します。
覚えておくべきキーポイント:
* 極性溶媒 一般に、非極性溶媒よりもイオン化合物の溶解により優れています。
* 静電力の強度 イオン化合物中のイオン間は、その溶解度に影響します。 強力な力は溶解度が低下します。
* 溶媒の極性 イオンと相互作用し、それらをバラバラにする能力に影響を与えます。
他に質問がある場合はお知らせください!