反応:
2h₂(g) +o₂(g)→2h₂o(l)
酸化:
* 水素(H₂)は酸化されています。 酸化は電子の損失です。 この反応では、各水素原子は電子を失い、水素イオン(H⁺)になります。
結合形成:
* 共有結合が形成されます。 水(H₂O)は、水素と酸素原子の間の電子の共有によって形成されます。 各酸素原子は、2つの水素原子で2つの電子を共有し、2つの共有結合を形成します。
説明:
1。反応物: 気体の水素(H₂)とガス酸素(O₂)は出発材料です。
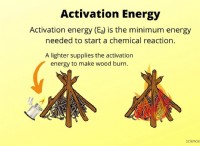
2。燃焼: 水素が燃焼すると、酸素と急速に反応し、熱と光の形でエネルギーを放出します。
3。電子伝達: 酸素よりも電気陰性度が低い水素原子は、電子を失い、正に帯電します(H⁺)。 酸素原子はこれらの電子を獲得し、負に帯電します(O²⁻)。
4。水の形成: 正に帯電した水素イオン(H⁺)と負に帯電した酸素イオン(O²⁻)は、互いに引き付けられ、共有結合を形成し、水分子(H₂O)を作成します。
概要:
* 酸化分子: 水素(H₂)
* 結合形成: 水分子内の共有結合(H₂O)