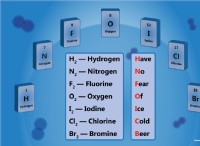
基本を理解する
* イオン化合物: 正の帯電イオン(陽イオン)と負に帯電したイオン(アニオン)の間の静電引力によって形成されます。これらには通常、金属と非金属が含まれます。
* 共有化合物: 原子が電子を共有して安定した電子構成を実現するときに形成されます。これらには通常、2つの非金属が含まれます。
キーインジケーター
1。電気陰性の差:
* イオン化合物: 大きな電気陰性度の差があります(通常は1.7を超える)。
* 共有化合物: 電気陰性度の差が小さくなります(1.7未満)。
2。要素の種類:
* イオン化合物: 通常、金属(陽イオン)と非金属(アニオン)が含まれます。
* 共有化合物: 通常、2つ以上の非金属が含まれます。
3。物理的特性:
* イオン化合物:
* 高融点と沸点 強い静電力のため。
* 室温で固体 (いくつかの例外を除く)。
* 水または溶融に溶けたときの電気の良い導体 。
* 共有化合物:
* 融点と沸点の低い イオン化合物より。
* 室温での固体、液体、またはガスになる可能性があります 。
* 電気導体が不十分 (いくつかの例外を除く)。
追加の考慮事項
* 多原子イオン: これらは、単一の荷電ユニットとして機能する原子のグループです。 それらは、イオン化合物と共有化合物の両方に見られます。
* 例外: ルールにはいくつかの例外があります。たとえば、伝統的にイオンと考えられていたいくつかの化合物は、共有特性を示すことがあり、その逆も同様です。
例
* イオン: NaCl(塩化ナトリウム)、MGO(酸化マグネシウム)、CaCl₂(塩化カルシウム)
* 共有結合: H₂O(水)、CO₂(二酸化炭素)、ch₄(メタン)
ルールを適用する方法
1。要素を識別します: それらは金属ですか、それとも非金属ですか?
2。電気陰性の違いを確認: 関係する要素の電気陰性度を調べます。
3。物理的特性を考慮してください: 該当する場合は、高い融点/沸点、室温での固体状態、および溶液中の導電率の証拠を探してください。
覚えておいてください: これらは一般的なガイドラインです。特定の要素プロパティについては、必ず定期的な表と電気陰性のチャートを参照してください。