1。化学的特性:
* 同様の電子構成: どちらも最も外側のシェルに6つの電子を持ち、安定したオクテット構成を実現するために2つの電子を獲得する傾向があります。
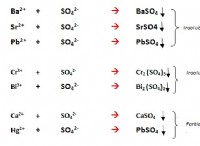
* アニオンの形成: どちらも、-2電荷(硫化物、s²⁻、および酸化物、o²⁻)を備えた負に帯電したイオン(陰イオン)を形成します。
* 酸化物の形成: どちらも酸素と反応して酸化物を形成します。たとえば、硫黄は二酸化硫黄(SO₂)と三酸化硫黄(SO₃)を形成しますが、酸素は他のさまざまな元素を備えた酸化物を形成します。
2。物理的特性:
* 室温での気体: 両方の要素は、室温のガスとして存在します。
* 淡黄色: 両方の要素は、固体状態で淡黄色に見えます。
* 電気の導体が悪い: どちらも電気と熱の導体が貧弱です。
3。生物学的重要性:
* 人生に不可欠: どちらも人生に不可欠です。酸素は呼吸に不可欠ですが、硫黄はアミノ酸、タンパク質、および多くの酵素の成分です。
4。使用:
* 産業用途: どちらも多数の産業用途があります。硫黄は、多くの産業で重要な化学物質である硫酸の生産に使用されています。酸素は、燃焼や鋼製造などのさまざまな産業プロセスで使用されます。
重要な違い:
類似点を共有している間、硫黄と酸素にも重要な違いがあります。
* 融点と沸点: 硫黄は、酸素よりも高い融点と沸点を持っています。
* 反応性: 酸素は硫黄よりも反応的です。
* 存在量: 酸素は、地球の大気中の硫黄よりもはるかに豊富です。
全体として、硫黄と酸素は、周期表での共有グループのために基本的な類似点を共有します。ただし、それらは、多様なアプリケーションを備えた明確な要素を作成する独自のプロパティも所有しています。